Este documento trata sobre la estereoquímica, que es el estudio de las moléculas en tres dimensiones. Explica conceptos como quiralidad, enantiómeros, diastereómeros, centros quirales, configuración absoluta R/S, proyecciones de Fischer, y diferentes tipos de isómeros como meso. También cubre moléculas con más de un centro quiral y cómo esto afecta el número de estereoisómeros posibles.





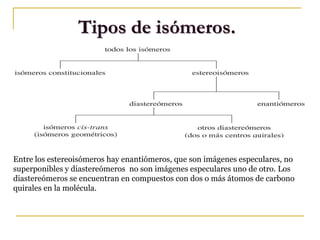

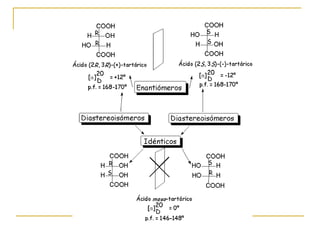
![¿Por qué en el caso del ácido tartárico (ácido 2,3-dihidroxibutanodioico),
con dos estereocentros, sólo se producen tres estereoisómeros?
(+)-tartaric acid: [α]D = +12º m.p. 170 ºC
(–)-tartaric acid: [α]D = –12º m.p. 170 ºC
meso-tartaric acid: [α]D = 0º m.p. 140 ºC
LA FORMA MESO](https://image.slidesharecdn.com/estereoquc3admica-clase-3-1er-semestre-2011-copy-150208192143-conversion-gate02/85/Estereoquimica-34-320.jpg)
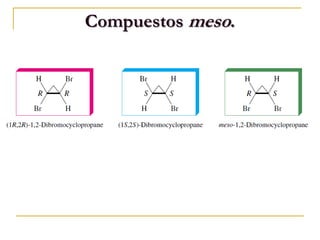
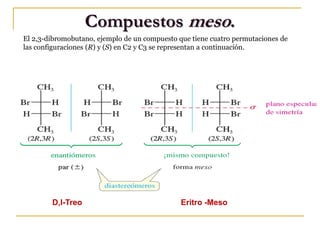
![Compuestos meso.
(+)-tartaric acid: [α]D = +12º m.p. 170 ºC
(–)-tartaric acid: [α]D = –12º m.p. 170 ºC
meso-tartaric acid: [α]D = 0º m.p. 140 ºC](https://image.slidesharecdn.com/estereoquc3admica-clase-3-1er-semestre-2011-copy-150208192143-conversion-gate02/85/Estereoquimica-35-320.jpg)