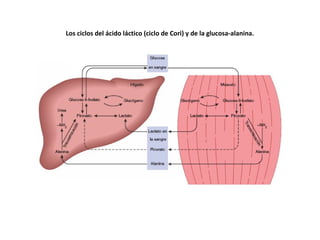
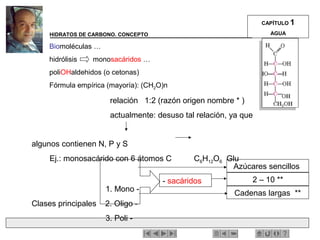
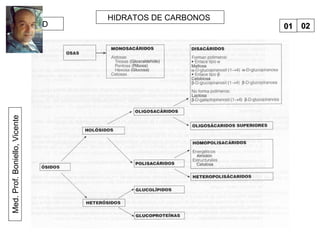
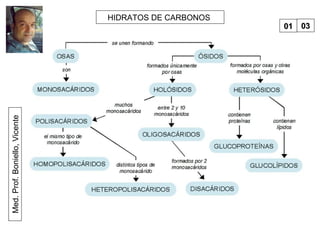
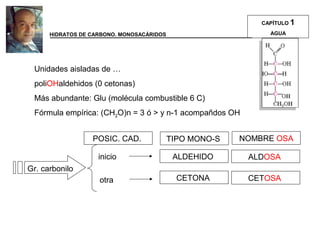
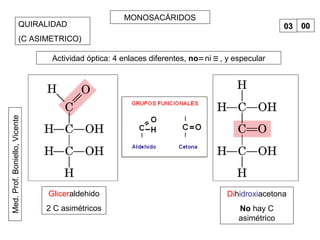
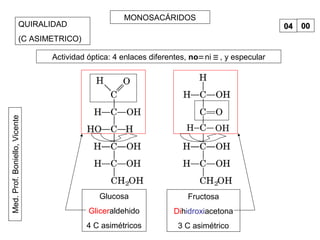
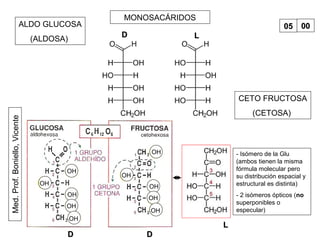
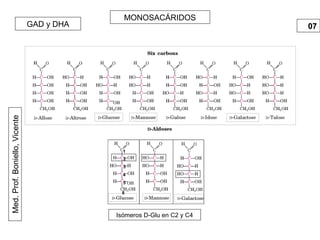
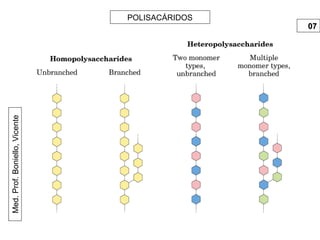
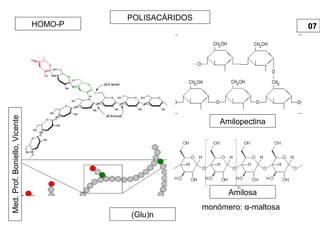
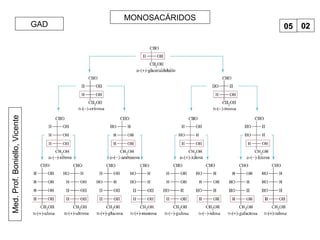
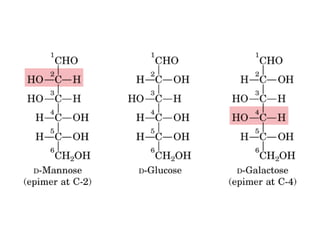
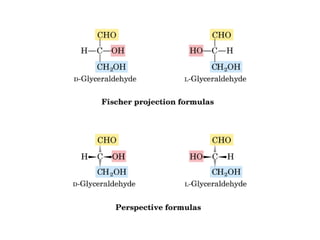
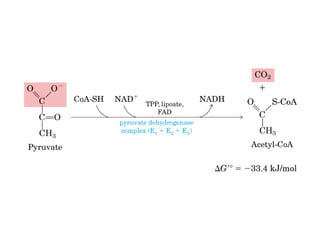
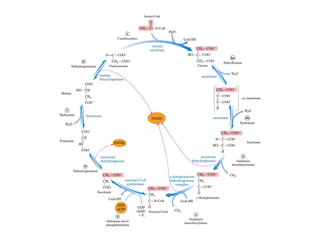
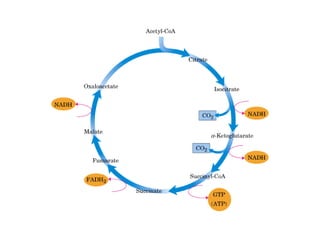
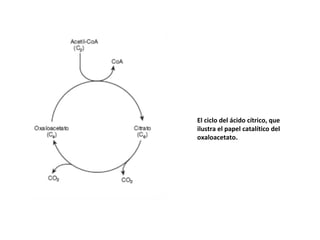
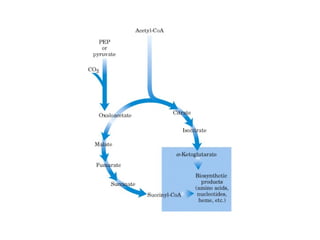
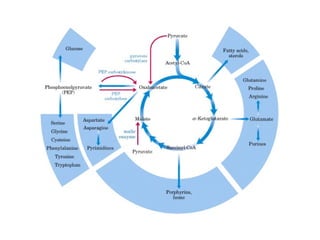
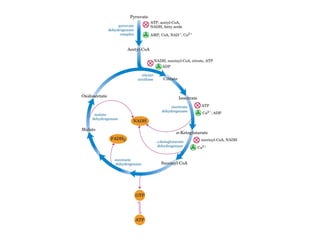
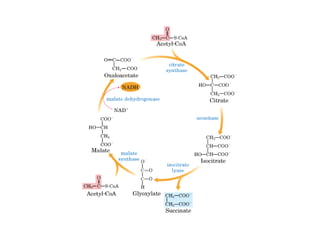
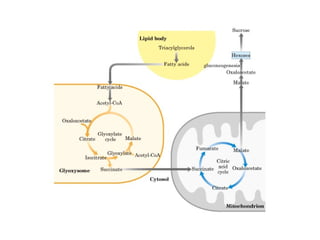
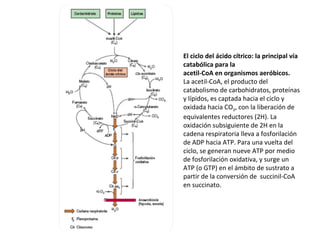
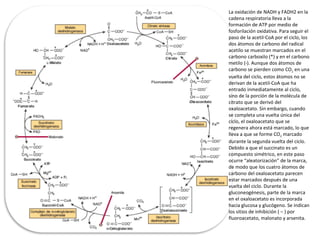
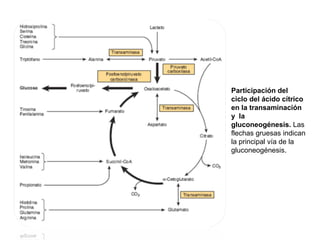
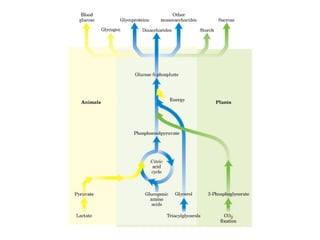
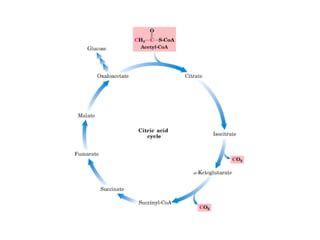
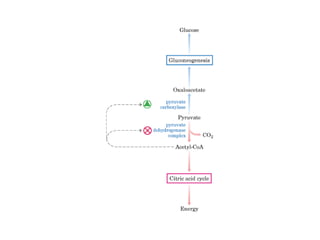
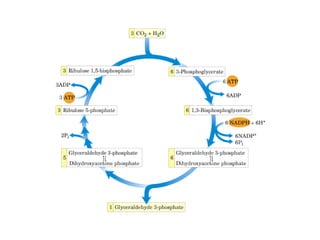
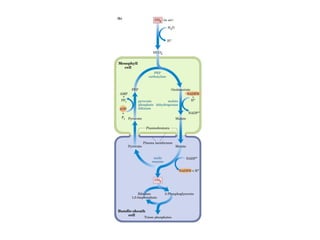
Este documento trata sobre biomoléculas como los hidratos de carbono. Explica que los monosacáridos son las unidades básicas y que pueden unirse para formar oligosacáridos y polisacáridos. También describe las principales rutas metabólicas de los carbohidratos como la glucólisis, la gluconeogénesis y el ciclo del ácido cítrico, el cual juega un papel importante en la oxidación de la acetil-CoA para producir energía.







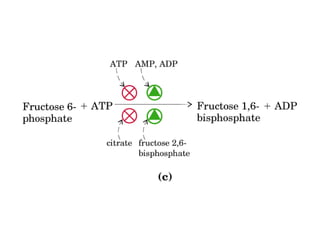
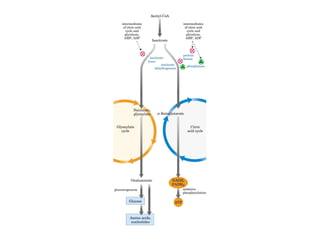
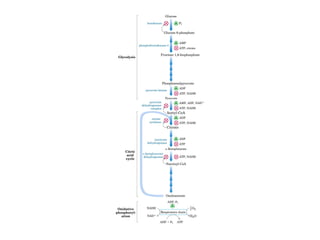
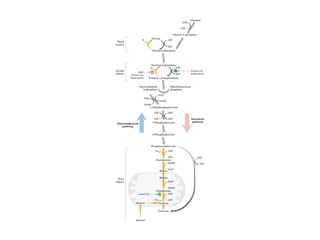
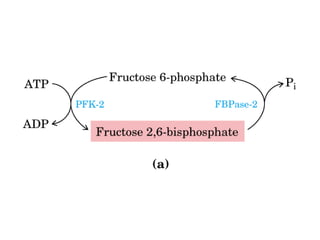
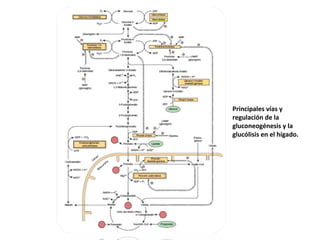
![Control de la glucólisis y la gluconeogénesis
en el hígado por medio de la fructosa 2,6-
bisfosfato y la enzima bifuncional PFK-2/F-
2,6-Pasa (6-fosfofructo-2-cinasa/ fructosa
2,6-bisfosfatasa). (PKF-1, fosfofructocinasa-
1 [6-fosfofructo-1-cinasa]; F-1,6-pasa,
fructosa 1,6-bisfosfatasa.) Las flechas
onduladas indican efectos alostéricos.](https://image.slidesharecdn.com/hidratosdecarbonoporvicenteboniello-resumen-161113020803/85/Hidratosdecarbonoporvicenteboniello-resumen-101-320.jpg)