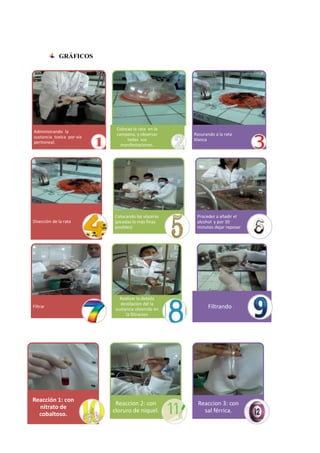
1. Las estudiantes Teresa Heras y Katherin Hoyos realizaron una práctica de laboratorio sobre la intoxicación por cadmio en cobayos. 2. Administraron cadmio por vía peritoneal a un cobayo y observaron que presentó inmovilidad y perdida de equilibrio, muriendo a los 2 minutos. 3. Mediante reacciones químicas comprobaron la presencia de cadmio en las vísceras del cobayo.














![SUSTANCIAS
HCl concentrado
Clorato de potasio
Hidróxido de sodio
Nitrato de Bismuto
Cloruro estannoso
Zinc metálico
Azul de metileno
PROCEDIMIENTO
Administrar 10 ml de cloruro estannoso por vía peritoneal al cobayo
Colocar al cobayo en la campana, y observando todas sus manifestaciones que
presenta hasta su muerte.
Rasurar el cobayo
Disección del cobayo.
Colocando las vísceras (picadas lo más finas posibles), en el recipiente adecuado
(Vaso de precipitación).
Colocar 25 ml de HCl concentrado.
Agregar 2gr de clorato de potasio.
Llevar a Baño María por 30 minutos
En el transcurso de 25 minutos agregar 2gr más de clorato de potasio.
Luego que ya haya culminado el proceso de Baño María, realizar una debida
filtración para obtener el líquido filtrado o muestra para realizar las debidas
reacciones de identificación.
4. Con el NaOH: A 1ml de solución de muestra, agregamos algunas gotas de NaOH,
con lo cual en caso positivo se debe formar un precipitado color blanco por formación
de Sn(OH)2. Este precipitado es soluble en exceso de reactivo por formación de
Estannito [Sn(OH)3]Sn++ + 2OH
Sn(OH)2
5. Con las sales de Bismuto. Al Estannito formado en la reacción anterior, agregarle
algunas gotas de sales de bismuto, en caso positivo se forma un precipitado color
negro bismuto metálico.
[Sn(OH)3]- + Bi+++
Bi metálico color negro
6. Con el Zinc metálico: Todos los metales que se encuentran por encima del Estaño en
la escala de fuerza electromotriz, reducen a los iones Sn+3 y Sn+2 a estaño metálico
color blanco en forma de cocos.](https://image.slidesharecdn.com/informesdepractica-140116231614-phpapp01/85/Informes-de-practica-16-320.jpg)