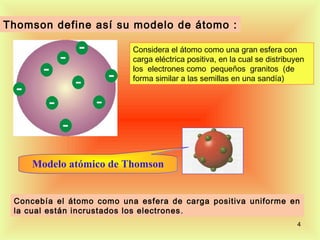
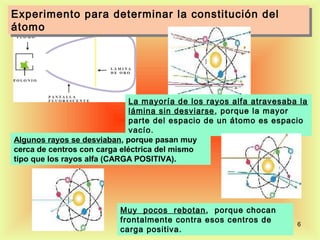
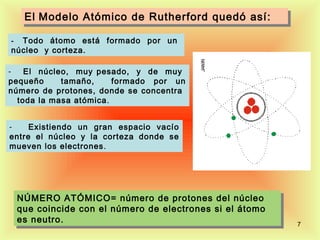
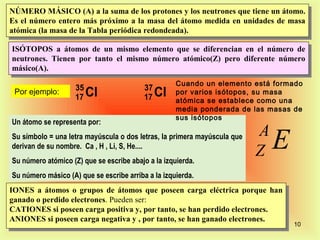
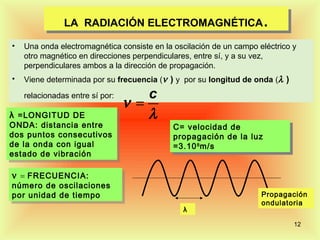
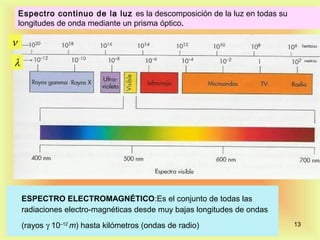
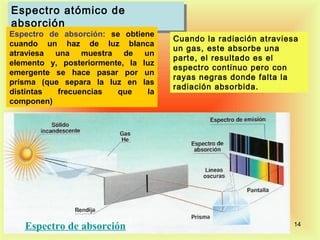
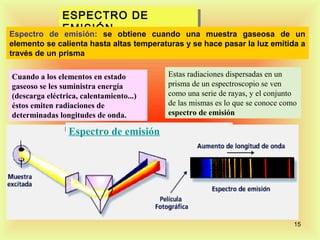
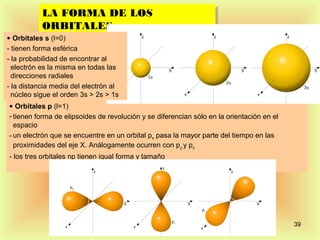
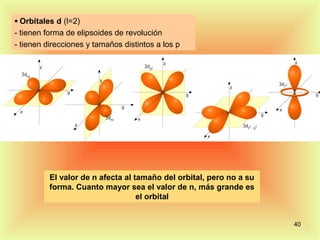
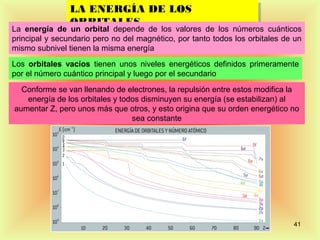
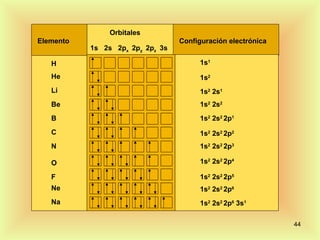
El documento describe la evolución del modelo atómico desde Dalton hasta Rutherford. Dalton propuso que los átomos son indivisibles e indestructibles y que los átomos de un mismo elemento tienen la misma masa. Thomson propuso un modelo de átomo con una esfera positiva con electrones distribuidos dentro. Rutherford descubrió mediante experimentos de dispersión que el átomo consiste principalmente en espacio vacío con un núcleo denso y pequeño en el centro donde se concentra la masa.