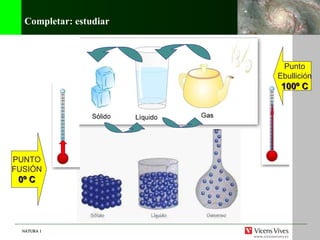
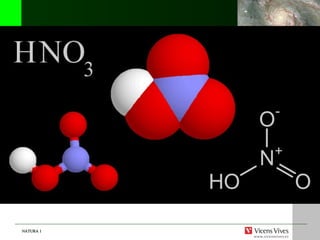
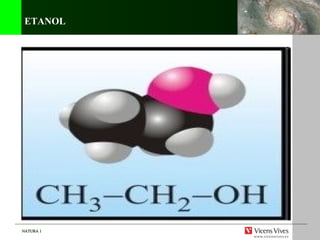
El documento habla sobre los diferentes estados de la materia, incluyendo sólido, líquido y gaseoso. Explica que la materia puede cambiar de estado a través de cambios de temperatura, como cuando el agua se convierte en hielo a 0°C o hierve a 100°C. También describe los átomos y moléculas que componen la materia, y diferentes tipos de materiales como metales, vidrio, plásticos y fibras que son de gran interés.