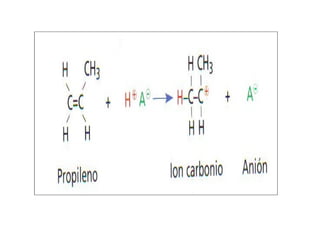
Este documento resume los diferentes tipos de polimerización, incluyendo adición, catiónica, aniónica, radicalaria y condensación. La polimerización por adición ocurre cuando monómeros con enlaces dobles u triples se unen en cadenas. La polimerización catiónica involucra un extremo catiónico en crecimiento, mientras que la radicalaria involucra radicales libres. La polimerización de condensación une monómeros que reaccionan para formar dímeros que se unen en cadenas indefinidamente. El document