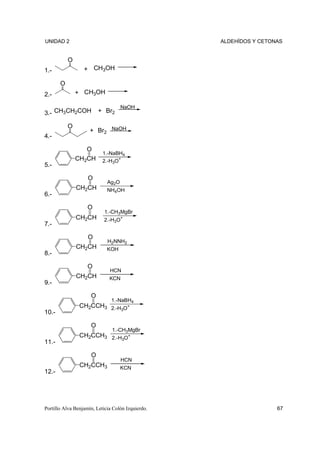
Este documento trata sobre aldehídos y cetonas. Explica la nomenclatura, estructura y propiedades de estos compuestos carbonílicos. También describe métodos comunes para la obtención de aldehídos, como la oxidación de alcoholes primarios y la oxidación controlada de metilbencenos.





![UNIDAD 2 ALDEHÍDOS Y CETONAS
aluminio desactivado LiAlH4 en forma de hidruro tri-terbutoxi de litio y aluminio,
LiAlH[O-C(CH3)3]3.
O O
H2
R ó (Ar) C Cl R ó (Ar) C H
Pd(BaSO4)
cloruro de acilo aldehído
O O
LiAlH[O-C(CH3)3]3
R ó (Ar) C Cl R ó (Ar) C H
cloruro de acilo aldehído
2.4.4 Hidrocarbonilación de alquenos (reacción 0X0)
Uno de los procesos para la síntesis de aldehídos se llama hidroformilación o
reacción oxo. En esta reacción un alqueno reacciona con monóxido de carbono e
hidrógeno, en presencia del catalizador de cobalto, HCo(CO4), como se presenta a
continuación:
HCo(CO)4
R HC CH2 + CO + H2 RCH2CH2CHO + isómeros
2000psi, 110-150ºC
2.4.5 Oxidación de alquenos (proceso wacker)
Los alquenos pueden oxidarse a varios productos, dependiendo del reactivo que se
use. Por lo que las reacciones de oxidación de un doble enlace C=C se pueden
clasificar en 2 tipos, el primer tipo corresponde a la oxidación del enlace pi sin
ruptura del enlace, el segundo tipo se refiere a la oxidación del enlace pi con ruptura
del enlace sigma; este último es el de interés para este punto ya que cuando en la
oxidación se rompen los enlaces π y σ se obtienen como productos a los aldehídos,
cetonas ó ácidos carboxílicos.
O
O3
C C R C H
Zn/ H+
aldehído
Portillo Alva Benjamín, Leticia Colón Izquierdo. 44](https://image.slidesharecdn.com/r53778-121018212756-phpapp02/85/R53778-8-320.jpg)
















![UNIDAD 2 ALDEHÍDOS Y CETONAS
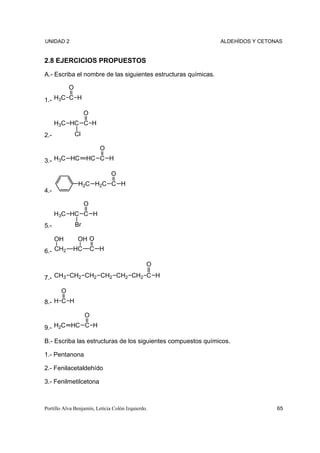
4.- 3,5-dimetilbenzaldehído
5.- 2-hidroxi-3-pentanona
C.- Indique otro nombre aceptable para cada uno de los siguientes compuestos.
1.- Dimetilcetona
2.- 1-fenil-2-butanona
3.- Etilisopropilcetona
4.- Dibencilcetona
5.- Etilvinilcetona
D.- Indique algunas semejanzas entre los aldehídos y las cetonas.
E.- ¿Cómo se pueden distinguir los aldehídos de las cetonas?
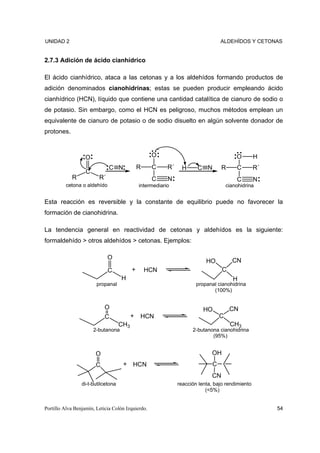
F.- Complete las siguientes reacciones
+ H2 Pd(BaSO4) (CH3)2CHCHO
1.-
CH3
H3C C C CH3 + NaIO
2.- CH3 O
O
HgSO4
+ H2O H2SO4
3.-
G.- Indique los pasos en las siguientes síntesis:
1.- Cloruro de acetilo a acetal
2.- Etanol a 2-buteno
H.- Los aldehídos reaccionan con el reactivo de Tollens [Ag(NH3)+2] pero no con las
cetonas, escriba un ejemplo y explique este hecho.
I.- Escriba la reacción de: (1) la butanona y (2) el butanal con HCN. Establezca el
mecanismo de estas reacciones.
J.- Complete las siguientes reacciones.
Portillo Alva Benjamín, Leticia Colón Izquierdo. 66](https://image.slidesharecdn.com/r53778-121018212756-phpapp02/85/R53778-30-320.jpg)