Aldehidos y cetonas
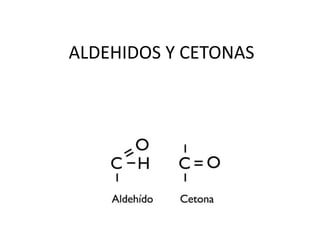
- 2. ESTRUCTURA • Los aldehídos y las cetonas: son compuestos caracterizados por la presencia del grupo carbonilo (C=O). Los aldehídos presentan el grupo carbonilo en posición terminal mientras que las cetonas lo presentan en posición intermedia.
- 3. PROPIEDADES FISICAS • La presencia del grupo carbonilo convierte a los aldehídos y cetonas en compuestos polares. Los compuestos de hasta cuatro átomos de carbono, forman puente de hidrógeno con el agua, lo cual los hace completamente solubles en agua. Igualmente son solubles en solventes orgánicos.
- 4. NOMENCLATURA • ALDEHIDOS Los aldehídos se nombran reemplazando la terminación -ano del alcano correspondiente por -al. No es necesario especificar la posición del grupo aldehído, puesto que ocupa el extremo de la cadena
- 5. • El grupo -CHO unido a un ciclo se llama - carbaldehído. La numeración del ciclo se realiza dando localizador 1 al carbono del ciclo que contiene el grupo aldehído.
- 6. • CETONAS Las cetonas se nombran sustituyendo la terminación -ano del alcano con igual longitud de cadena por -ona. Se toma como cadena principal la de mayor longitud que contiene el grupo carbonilo y se numera para que éste tome el localizador más bajo.
- 7. • Existe un segundo tipo de nomenclatura para las cetonas, que consiste en nombrar las cadenas como sustituyentes, ordenándolas alfabéticamente y terminando el nombre con la palabra cetona.
- 8. SINTESIS DE ALDEHIDOS Y CETONAS • OXIDACION DE ALCOHOLES Los alcoholes primarios y secundarios se oxidan para dar aldehídos y cetonas respectivamente. Deben tomarse precauciones en la oxidación de alcoholes primarios, puesto que sobreoxidan a ácidos carboxílicos en presencia de oxidantes que contengan agua. En estos caso debe trabajarse con reactivos anhídros, como el clorocromato de piridino en diclorometano (PCC), a temperatura ambiente
- 9. Los alcoholes secundarios dan cetonas por oxidación. Se emplean como oxidantes permanganato, dicromato, trióxido de cromo. La oxidación supone la pérdida de dos hidrógenos del alcohol. Los alcoholes terciarios no pueden oxidar puesto que carecen de hidrógeno sobre el carbono.
- 10. • OZOONOLISIS DE ALQUENOS • Los alquenos rompen con ozono formando aldehídos y/o cetonas. Si el alqueno tiene hidrógenos vinílicos da aldehídos. Si tiene dos cadenas carbonadas forma cetonas.
- 11. • La ozoonólisis de alquenos cíclicos produce compuestos dicarbonílicos: Los alquenos terminales rompen formando metanal, que separa fácilmente de la mezcla por su bajo punto de ebullición.
- 12. • HIDRATACIONDE ALQUINOS Los alquinos se pueden hidratar Markovnikov, formando cetonas, o bien antiMarkovnivov, para formar aldehídos.
- 13. • REACCION DE FRIDEK-CRAFTS La introducción de grupos acilo en el benceno permite la preparación de cetonas con cadenas aromáticas.
- 14. SINTESIS CON ACIDOS ORGÁNICOS O SUS DERIVADOS • La reacción original incluía dos sustituciones nucleofílicas con grupo acilo: • la conversión de un cloruro de ácido en una N, O-dimetilhidroxiamida, conocida como amida de Weinreb, el tratamiento posterior de la amida de Weinreb con un reactivo organometálico, como un reactivo de Grignard o un reactivo de organolitio .
- 16. SINTESIS DE ACÉTO ACÉTICA • acetoacetato de etilo es alquilado en carbono α de ambos grupos carbonilo y luego es convertido en una cetona, o más específicamente, en una acetona sustituida en α.
- 17. COMPORTAMIENTO QUIMICO DE CETONAS • adición nucleofílica: Estas reacciones se producen frente al (reactivo de Grignard), para dar origen a un oxihaluro de alquil-magnesio que al ser tratado con agua da origen a un alcohol. Los aldehídos forman alcoholes secundarios.
- 18. • La reacción de adición nucleofílica en las cetonas dan origen a alcoholes terciarios.
- 19. REACTIVOS DE GRIGNARD • El reactivo de Grignard reacciona con el grupo C=O de aldehídos o cetonas para dar un intermediario tetraédrico que es un alcóxido de magnesio El intermediario se hidroliza para producir un alcohol neutro El reactivo de Grignard reacciona como un carbanión
- 20. ADICION DE AMINAS • La adición nucleofílica de una amina primaria para dar un intermediario tetraédrico: carbinolamina • Eliminación de agua para formar un nuevo enlace • Adición nucleofílica de una amina secundaria para dar un intemediario tetraédrico: carbinolamina • Eliminación de agua produce un ion iminio • Pérdida de un protón del átomo de carbono α- produce la enamina C=Nu
- 21. • Reacciones de condensación aldólica: En esta reacción se produce la unión de dos aldehídos o dos cetonas en presencia de una solución de NaOH formando un polímero, denominado aldol.
- 22. Condensacion knovenagel • la adición nucleófila sobre el carbonilo, de un aldehído o cetona, de un carbono activado (ácido) situado entre dos grupos aceptores de electrones
- 23. Reacción de Perkin • Utilizada para sintetizar derivados del ácido cinámico, por ejemplo ácidos aromáticos α,β- insaturados por una condensación aldólica de benzaldehídos y un anhídrido carboxílico en la presencia de una sal alcalina del ácido.
- 24. • Reacciones de sustitución en Alfa ocurrren en el carbono inmediato al carbono carbonilo: la posición α • Un hidrógeno α es sustituido por un electrófilo
- 25. • La Reacción de Cannizzaro • consiste en la dismutación de un aldehído sin hidrógeno en alfa (no enolizable) catalizado por una base.
- 26. • El reactivo de Tollens es un complejo acuoso de diamina-plata, presentado usualmente bajo la forma de nitrato.
- 27. REACCION DE FEHLING • El ensayo con el licor de Fehling se fundamenta en el poder reductor del grupo carbonilo de un aldehído. Éste se oxida a un ácido carboxílico y reduce la sal de cobre (II) en medio alcalino a óxido de cobre(I), que forma un precipitado de color rojo.
- 28. REACCION DE CLEMMENSEN • se reduce una cetona o un aldehído a un alcano usando amalgama de zinc y mercurio (Hg), además ácido clorhídrico para darle el medio ácido.
- 29. REACCION DE WOLFF- KISHNER • La reducción de Wolff-Kishner es una reacción química que reduce completamente una cetona (o aldehído) a un alcano
- 30. ACIDOS CARBOXILICOS Los ácidos carboxílicos constituyen un grupo de compuestos, caracterizados porque poseen un grupo funcional llamado grupo carboxilo o grupo carboxi (–COOH). Se puede representar como -COOH ó -CO2H. Donde R puede ser un alifático, aromático o cíclico .
- 31. Propiedades físicas • Los ácidos carboxílicos presentan puntos de ebullición elevados estos son el resultado de la formación de puentes de hidrógeno (dímeros). • Son solubles en solventes con menor polaridad como éter alcohol etc. • Son líquidos hasta los 9 átomos de carbono el resto son sólidos. • Incoloros Los ácidos carboxílicos de menor peso molecular son solubles en agua y a medida que aumenta el número de carbonos disminuye su solubilidad.
- 32. Propiedades químicas - Son ácidos débiles que se hallan parcialmente disociados en solución - -El carácter acido disminuye con el numero de carbonos - -reaccionan con los metales alcalinos para formar sales - -con los alcoholes forman ésteres - -al combinarse con amoniaco forman amidas - La acidez :estabilidad del ion carboxilato • ACIDOS CARBOXILICOS IMPORTANTES • Ácido metanoico • Ácido fórmico • Acido acético • Ácido benzoico • Ácido salicílico • Acido cítrico
- 33. Nomenclatura IUPAC - Se nombran anteponiendo la palabra "ácido" al nombre del hidrocarburo del que proceden y con la terminación "-oico". Cuando el ácido tiene sustituyentes, se numera la cadena dando el numero más bajo al carbono del grupo ácido. Los ácidos carboxílicos son prioritarios frente a otros grupos, que pasan a nombrarse como sustituyentes.
- 34. • Los ácidos carboxílicos también son prioritarios frente a alquenos y alquinos. En las moléculas con dos grupos ácido se nombran con la terminación -dioico. • Cuando el grupo ácido va unido a un anillo, se toma el ciclo como cadena principal y se termina en -carboxílico.
- 35. sintesis
- 36. Oxidación aldehídos a ácidos carboxilo
- 37. Oxidación de alquenos a ácidos carboxílicos los alquenos son fácilmente oxidados con permanganato de potasio, ozono, tetroxido de osmio etc.
- 38. Oxidación de alquil bencenos • El permanganato y el dicromato de potasio en caliente oxidan alquilbencenos a ácidos benzoicos. Esta reacción sólo es posible si en la posición bencílica existe al menos un hidrógeno. No importa la longitud de las cadenas o si son ramificadas todas rompen por la posición bencílica generando el grupo carboxílico. Sin hidrógenos en la posición bencílica no se produce la ruptura