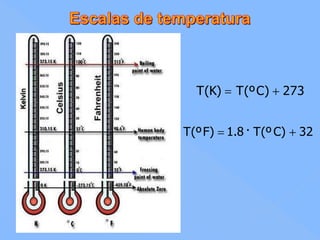
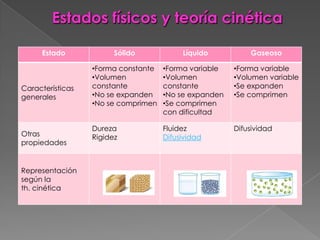
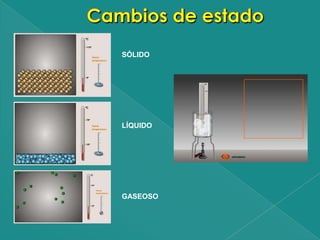
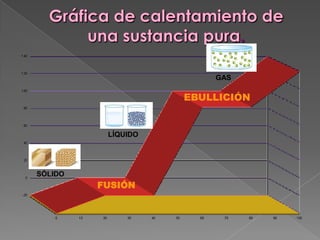
El documento describe los tres estados físicos de la materia: sólido, líquido y gaseoso. Los gases están compuestos de partículas muy pequeñas que se mueven rectilíneamente y de forma uniforme, ocupando todo el volumen del recipiente y ejerciendo presión por colisiones con las paredes. La temperatura de un gas depende de la energía cinética promedio de sus partículas. Los sólidos mantienen una forma constante mientras que los líquidos y gases varían su forma para ocupar el espacio del recipient