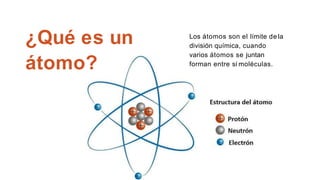
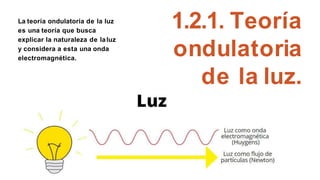
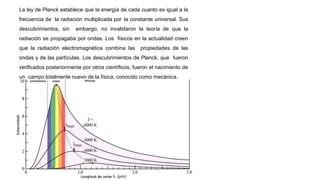
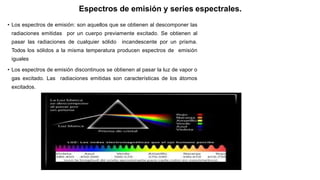
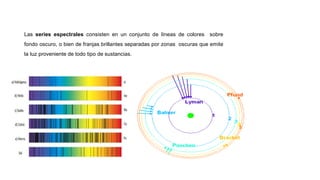
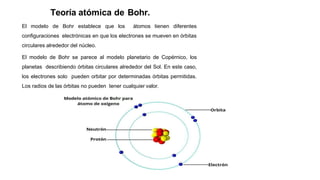
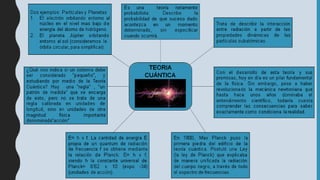
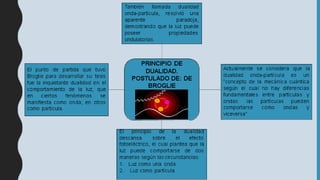
Este documento presenta información sobre la teoría cuántica y la estructura atómica. Explica conceptos como las partículas subatómicas, la radiactividad, la teoría ondulatoria de la luz, el efecto fotoeléctrico, los espectros de emisión, los modelos atómicos de Bohr y Sommerfeld, la teoría cuántica, el principio de incertidumbre de Heisenberg, la ecuación de Schrödinger, los números cuánticos y los orbitales atómic