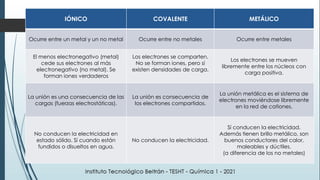
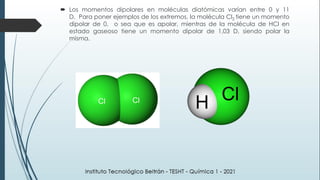
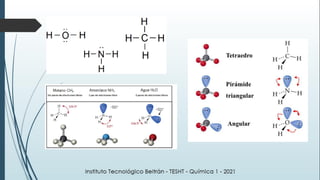
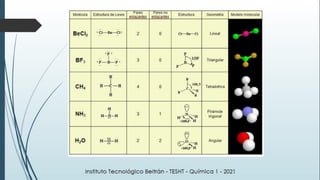
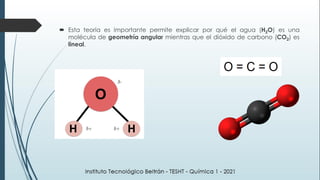
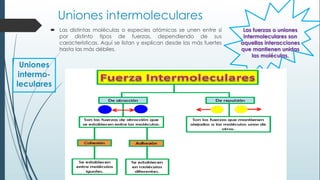
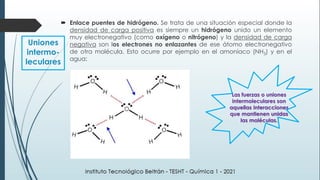
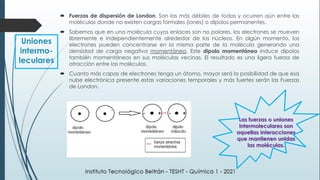
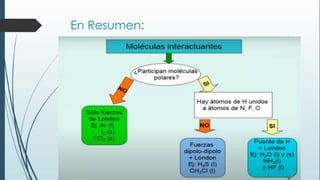
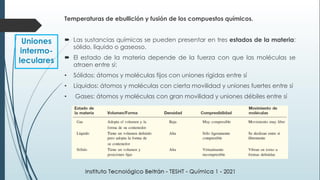
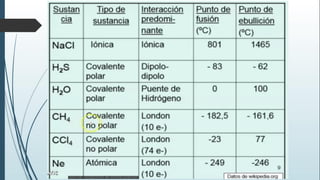
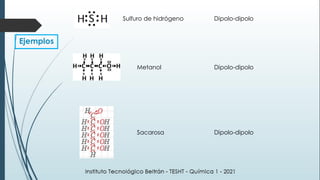
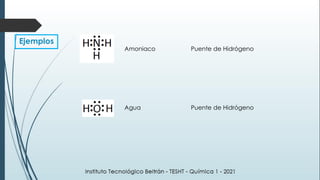
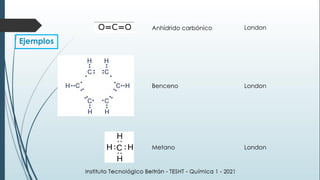
Este documento resume una lección de química sobre uniones químicas. Explica los tipos de enlaces químicos iónico, covalente y metálico. Luego describe la teoría de repulsión de pares de electrones de valencia y cómo esto determina la geometría molecular. Finalmente, define varios tipos de uniones intermoleculares como puentes de hidrógeno, dipolo-dipolo e interacciones de dispersión de London. Incluye ejemplos para ilustrar estos conceptos.