Grupos amino
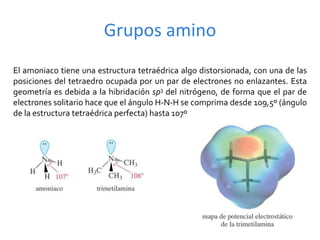
- 1. El amoniaco tiene una estructura tetraédrica algo distorsionada, con una de las posiciones del tetraedro ocupada por un par de electrones no enlazantes. Esta geometría es debida a la hibridación sp3 del nitrógeno, de forma que el par de electrones solitario hace que el ángulo H-N-H se comprima desde 109,5º (ángulo de la estructura tetraédrica perfecta) hasta 107º Grupos amino
- 2. Según se sustituyan uno, dos o tres hidrógenos, las aminas serán primarias, secundarias o terciarias, respectivamente. Amoníaco Amina primaria Amina secundaria Amina terciaria Grupos amino
- 3. Las aminas son fuertemente polares debido a que el gran momento dipolar del par de electrones solitario se suma a los momentos dipolares de los enlaces C-N y H-N El enlace de hidrógeno N-H es más débil que el enlace de hidrógeno O-H, por tanto las aminas tienen puntos de ebullición más bajos que los alcoholes con masas moleculares similares Grupos amino
- 4. N R H H N R HH N R H H N R H H O H H O H H O HH N R H H Asociación por puente de hidrógeno de aminas 1rias Puente de hidrógeno intramolecular entre una amina 1ria y el agua Aceptacion de un protón mediante un enlace de hidrógeno entre el agua y una amina 3ria. O H H N R R R Grupos amino
- 5. La naturaleza polar del enlace N-H provoca la formación de puentes de hidrógeno entre las moléculas de las aminas Implicaciones: -Altos puntos de fusión y ebullición comparados con los alcanos -Alta solubilidad en medio acuoso Compuesto P.eb. P.f. Compuesto P.eb. P.f. CH3CH2CH3 -42º -188º (CH3)3N 3º -117º CH3CH2CH2NH2 48º -83º (CH3CH2CH2)2NH 110º -40º CH3CH2CH2OH 97º -126º (CH3CH2CH2)3N 155º -94º Grupos amino
- 6. Compuesto Tipo Peso molecular Punto de ebullición (°C) (CH3)3N Amina terciaria 59 3 CH3-NH-CH2-CH3 Amina secundaria 59 37 CH3-O-CH2-CH3 Éter 60 8 CH3CH2CH2-NH2 Amina primaria 59 48 CH3CH2CH2-OH Alcohol 60 97 Grupos amino
- 7. Una amina es un nucleófilo (una base de Lewis) debido a que el par solitario de electrones no enlazantes pueden formar un enlace con un electrófilo. Una amina también puede actuar como base de Brönsted-Lowry, aceptando un protón de un ácido Cuando una amina actúa como un nucleófilo, se forma un enlace N-C. Cuando actúa como una base, se forma un enlace N-H Grupos amino
- 8. Grupos amino
- 9. Grupos amino
- 10. La mayoría de las aminas, que contienen más de seis átomos de carbono, son relativamente insolubles en agua. En presencia de ácido diluido (en disolución acuosa), estas aminas forman las sales de amonio correspondientes, por lo que se disuelven en agua. Cuando la solución se transforma en alcalina, se regenera la amina La amina regenerada o bien se separa de la solución acuosa, o se extrae con un disolvente orgánico Grupos amino
- 11. La mayoría de las aminas, que contienen más de seis átomos de carbono, son relativamente insolubles en agua. En presencia de ácido diluido (en disolución acuosa), estas aminas forman las sales de amonio correspondientes, por lo que se disuelven en agua. La formación de una sal soluble es una de las características de las pruebas para el grupo funcional amina Una amina puede convertirse en sal de amonio mediante un tratamiento con ácido. La sal de amonio es soluble en agua. Al tratar la sal de amonio con soluciones básicas la volverá a convertir en la amina Grupos amino
- 12. Varios grupos funcionales en una sola molécula
- 13. Varios grupos funcionales en una sola molécula
- 14. Varios grupos funcionales en una sola molécula
- 15. Varios grupos funcionales en una sola molécula
- 16. Varios grupos funcionales en una sola molécula
- 17. Varios grupos funcionales en una sola molécula
