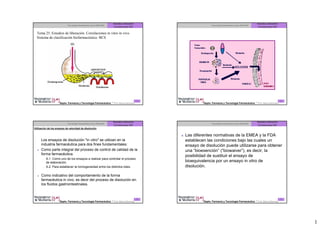
Estudios de liberacion
- 1. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Tema 25. Estudios de liberación. Correlaciones in vitro in vivo Sistema de clasificación biofarmacéutico. BCS 1 2 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Utilización de los ensayos de velocidad de disolución Las diferentes normativas de la EMEA y la FDA establecen las condiciones bajo las cuales un Los ensayos de disolución quot;in vitroquot; se utilizan en la industria farmacéutica para dos fines fundamentales: ensayo de disolución puede utilizarse para obtener Como parte integral del proceso de control de calidad de la una “bioexención” (“biowaiver”), es decir, la forma farmacéutica. posibilidad de sustituir el ensayo de − A.1. Como uno de los ensayos a realizar para controlar el proceso bioequivalencia por un ensayo in vitro de de elaboración. disolución. − A.2. Para establecer la homogeneidad entre los distintos lotes. Como indicativo del comportamiento de la forma farmacéutica in vivo, es decir del proceso de disolución en los fluidos gastrointestinales. 3 4 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 1
- 2. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV La velocidad de disolución se puede definir como Metodología de los ensayos de disolución la cantidad de fármaco que se disuelve en cada las condiciones experimentales de los ensayos de unidad de tiempo, a partir de una forma sólida de disolución son diferentes en función del objetivo dosificación deseado. condiciones estándar de temperatura, composición Factores a considerar en el diseño de un ensayo del medio e interfase sólido/líquido. de disolución El ensayo debe realizarse en condiciones de − Composición del medio mínima concentración, condiciones sumidero o de gradiente máximo (quot;sinkquot; ), de modo que la − Temperatura concentración de fármaco en el fluido de disolución − Agitación no rebase nunca el 20% de su concentración a − Duración, toma de muestras. saturación 5 6 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 7 8 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 2
- 3. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 9 10 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Filter Head Aparato USP 4. Prueba de Disolución de la USP Glass Prueba de Disolución de la USP Dispositivo de flujo Microfiber • Corresponde a un ensayo oficial. Filter continuo • Originalmente se introdujo para formas farmacéuticas sólidas Cylindrical section (comprimidos, cápsulas). Con el tiempo se han incorporado en la monografía de otros productos (gránulos, supositorios, Piston Pump Mesh ungüentos, parches transdérmicos, etc. Filter • La USP define como “Q” al % de fármaco disuelto a un Bead tiempo “t” determinado para medicamentos de liberación convencional y en más de un tiempo para preparados de Peristaltic Pump liberación controlada. Los resultados se expresan en función de la potencia declarada del producto (100%). • Se acepta un lote de producción si los resultados satisfacen Uv-Vis los criterios establecidos en tablas de aceptación de la USP. Spectrophotometer Dissolution medium 11 12 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 3
- 4. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Estudios de Cinética de Disolución Tabla de aceptación para preparados convencionales La PRUEBA DE DISOLUCION de Farmacopea no FASE NUMERO DE CRITERIO DE ACEPTACION corresponde a un estudio cinético propiamente tal. UNIDADES Corresponde a la determinación de uno o dos puntos Cada unidad no es menor que Q+5% S1 6 experimentales (% disuelto a un tiempo “t”) El promedio de 12 unidades (S1+ S2) es igual o S2 6 EL PERFIL DE DISOLUCION completo se requiere mayor que Q y ninguna unidad es menor que Q- 15% para: El promedio de 24 unidades (S1+S2 +S3) es igual o mayor que Q; no más de dos unidades • Determinar el orden y la constante de velocidad de S3 12 son menores que Q-15% y ninguna unidad es disolución (Kd) menor que Q-25% • Determinar el tiempo de latencia (TL) Q = Cantidad de fármaco disuelto x 100 = % disuelto • Determinar cambios en el proceso de disolución Cantidad declarada • Establecer una Bioexención mediante BCS 13 14 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Ir a herramientas de cálculo de MB Modelos con base fisicoquímica − Superficie sólida constante: • Orden cero − Superficie variable • Orden uno • Raíz cúbica • Raíz cuadrada Sin base fisicoquímica − Ecuación de Weibull 15 16 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 4
- 5. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 17 18 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 19 20 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 5
- 6. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Weibull b=1---Primer orden 21 22 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Cinética de orden cero: tiempo (mins) (Cantidad mg) Pred Primer orden Resduales^2 Pred Weibull Residuales^2 18 11.98 69.74 3335.94 11.99 0.00 Habitual en formas farmacéuticas que no se disgregan bajo el 36 43.21 129.75 7488.93 43.29 0.01 54 88.86 181.39 8561.71 88.85 0.00 supuesto de que la superficie permanece constante durante la 72 143.41 225.83 6793.26 143.39 0.00 90 201.69 264.07 3890.51 201.67 0.00 liberación del fármaco. 108 259.12 296.97 1433.03 259.09 0.00 126 312.13 325.29 173.23 312.09 0.00 Cinética de primer orden 144 358.20 349.66 72.95 358.36 0.02 162 396.80 370.63 684.74 396.77 0.00 180 427.25 388.67 1488.38 427.23 0.00 La velocidad de liberación es proporcional a la cantidad de 198 450.50 404.20 2143.72 450.36 0.02 216 467.25 417.56 2468.61 467.23 0.00 fármaco remanente en la forma farmacéutica, asi pues la 234 479.02 429.06 2496.04 479.06 0.00 252 487.04 438.95 2312.70 487.04 0.00 velocidad de disolución disminuye con el tiempo. 270 492.23 447.47 2003.90 492.23 0.00 288 495.60 454.80 1665.02 495.49 0.01 Ecuación de Weibull : 306 497.46 461.10 1322.11 497.46 0.00 324 497.00 466.53 928.68 498.61 2.60 a: define la escala temporal del proceso, a=Tdb siendo Td el 342 499.27 471.19 788.09 499.27 0.00 360 499.80 475.21 604.56 499.62 0.03 tiempo necesario para disolver el 63.2% del fármaco en la forma SC= 50656.12 SC= 2.70 farmacéutica. b= factor de forma. kd= 0.01 a= 1.899988653 b= 10001.13046 La ecuación de primer orden es un caso particular de la ecuación AIC= 218.66 AIC= 23.89 r= 0.9912 1.0000 de weibull cuando b=1 23 24 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 6
- 7. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Selección de modelo cinético: SC, R, AIC, F snedecor 600.00 500.00 Par EE CV% par EE CV% Parametro EE QINF 79.33 4.02 5.06 QINF 78.903599 2.168806 2.75 QINF 75.152774 1.581212 400.00 exp cantidad TD 8.21 0.97 11.77 KD 0.122835 0.010862 8.84 KD 0.153178 0.009294 BETA 0.97823 0.155308 15.88 300.00 PrimerOrdenPred weibull 200.00 CSS 61823.3 CSS 61823.3 CSS 61823.3 WCSS 61823.3 WCSS 61823.3 WCSS 61823.3 SSR 5715.82 SSR 5717.05 SSR 5840.81 100.00 WSSR 5715.82 WSSR 5717.05 WSSR 5840.81 S 8.40034 S 8.34986 S 8.43975 0.00 DF 81 DF 82 DF 82 0 100 200 300 400 CORR_(OBS 0.9527 CORR_(OBS, 0.9526 CORR_(OBS 0.9517 AIC 732.68348 AIC 730.70146 AIC 732.50046 SC 739.97593 SC 735.5631 SC 737.36209 tiempo Weibull Primer Orden Raiz Cubica Weibull vs FO Fcalc numerador 1.23 Fcalculado 0.0174 Ftabul(0.05,1,81) 3.95885991 F (SC1-SC2/SC2)*(df2/df1-df2) denom 70.5657 p 0.8953 0.0500 Diferencias Fcalculada 337300.92 No Significativas Weibull vs Raiz Fcalc numerador 124.99 Fcalculado 1.771 Ftabul(0.05,1,81) 3.95885991 Ftabulada 4.41 denom 70.565679 p 0.1870 Diferencias No Significativas Fcal<Ftab El modelo mas complejo NO es mejor Fcal>Ftab El modelo mas complejo SI es mejor Conclusion SI es Mejor 25 26 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Dissolution curve comparison Model independent parameters Model independent approach: Time to dissolve a fixed % of the dose − f1: difference factor 1. Realizar el perfil de Dissolution efficiency DE T − f2 similarity factor AUC0 DE % = disolución de Problema y − AUCT0 Trapezoidal area of the dissolution Q100 ⋅ T curve from 0 to T(last point) Referencia (12 unidades). ⎧⎡ 1 n ⎫ − Q100*T=area of the rectangle Q∞-T −0.5 2⎤ ⎪ ⎪ 2. Usar los valores f2 = 50⋅ log⎨⎢1+ ⋅ ∑( Rt −Tt ) ⎥ ⋅100⎬ medios de los porcentajes ⎩⎣ ⎦ ⎪ ⎪ n t=1 ⎭ disueltos a cada tiempo ⎧ ⎫ n ⎪∑ Rt −Tt ⎪ para calcular el factor f2 ⎪ t=1 ⎪ 3. valores mayores de 50 f1 = ⎨ n ⎬⋅100 (entre 50 y 100) aseguran ⎪ ∑Rt ⎪ ⎪ t=1 ⎪ ⎩ ⎭ similitud o equivalencia de las curvas de los dos Statistical moments: MDT productos 27 28 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 7
- 8. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV A f2 value ≥50 ensures sameness of the two Three to four or more Curve comparison dissolution data points curves. (An average difference between two availables 120.00 profiles of 10% at all sampling data points 100.00 Coefficient of variation of % dissolved corresponds to an f2 value of 50) 80.00 the earlier data points less 60.00 than 20% and in later data 40.00 100 points not more of 10% f2 20.00 0.00 50 Same data points for 0 50 100 150 200 250 300 reference and test time (min) 10 Average difference % % medio 2% 5% 10% 15% 20% diferencia Only one data point after 85% dissolution of one of the products F2 83 65 50 41 36 29 30 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Dissolution test 1 t =n ⋅ ∑ ( Rt − Tt ) 2 B = A= f 2 = 50 ⋅ log10 (100 ⋅ C ) A + 1 C = 1/ B Quality control: n t =1 (R-T)2 Tmin Ref Test − Process control 5 14.6 11.5 9.6 Keep It Short and Simple − Batch-to-batch quality 10 23.7 21.1 6.8 Predictor of Product performance In vivo 15 34.7 31.3 11.6 20 44.2 38.4 33.6 N=8 25 51.9 45.1 46.2 BCS 30 58.1 51.0 50.4 45 73.4 65.8 57.8 60 85.6 84.1 2.3 90 105.5 97.5 64.0 120 105.7 97.5 67.2 31 32 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 8
- 9. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Dissolution test Biowaiver: permission to use dissolution test as a surrogate of pharmacokinetic data: i.e a waiver of the in vivo assays. For accepting product sameness under SUPAC- related changes. To waive in vivo bioequivalence requirements for lower strengths of a dosage form. To support waivers for other bioequivalence requirements. 33 34 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV In vitro Dissolution Amount Released % 120.0 The main objective of developing and evaluating 100.0 80.0 60.0 an IVIVC is to establish the dissolution test as a 40.0 20.0 0.0 surrogate for human bioequivalence studies, 0 100 200 300 time (min) which may reduce the number of bioequivalence IVIVC Plasma levels 100 studies performed during the initial approval 50 Amount absorbed % 80 40 plasma conc. process as well as with certain scale-up and post 30 60 20 10 approval changes. 40 0 0 100 200 300 400 20 time(min) 0 In vivo Absorption 0 20 40 60 80 100 Amount dissolved % A m o un t a bsor. % 120.0 100.0 80.0 60.0 Wagner-Nelson 40.0 20.0 Loo-Riegelman 0.0 0 100 200 300 Deconvolution.. time (min) 35 36 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 9
- 10. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV J = P ⋅C Solubility and Permeability Dissolution rate In vivo Luminal degradation •Same dissolution profile •Formulation components do not alter permeability or intestinal transit Amidon GL. Lennernas H. Shah VP. Crison JR. A theoretical basis for a biopharmaceutic drug classification: the correlation of in vitro drug product dissolution and in vivo bioavailability. Pharm. Res. 12(3):413-20, 1995 37 38 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Permeability classification What is a good permeability? Class I:HS/HP Class II:LS/HP How can we estimate intestinal permeability? Verapamil, Proparanolol Carbamazepine, Metoprolol Ketoprofen, Naproxen Permeability Class III:HS/LP Class IV: LS/LP F = Fa⋅ (1− Eg ) ⋅ (1− Eh) Ranitidine, Cimetidine, Furosemide, Eg= gut first-pass effects Atenolol Hydrochlorothiazide Eh= liver first-pass effects Volume of aqueous buffer to dissolve the highest dose 39 40 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 10
- 11. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Permeability H. Lennernas etal. 41 42 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 43 44 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 11
- 12. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Caco-2 monoloayers Apical Basolateral Permeability in Rat Jejunum and Fabs In Humans flux (AP) flux (BL) ΔQ = Pef ⋅ C ⋅ S Δt Apical chamber Cell monolayer Cell Basolateral chamber slope=b Accumulated Amounts time b=slope A=insert surface C=initial concentration Amidon, etal., Pharm. Res.,5 651, 1988 45 46 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Fa = 1 − e−(2⋅ An ) Absorption number An ⎛ Peff ⎞ Tres An = ⎜ ⎟ ⋅ (Tres ) = ⎜R ⎟ ⎝ ⎠ Tabs A high Permeability value ensures that the drug is completely absorbed during its residence time in intestine. (in absence of formulation factors) 47 48 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 12
- 13. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Exemption criteria of IN VIVO studiesUE Solubility: How much is enough? High solubility: Dissolution and solubility in what? − When the active substance is highly soluble, the product could be in general exempted from in vivo BE studies. − The amount contained in the highest dose strength of an IR product is dissolved in 250 mL of each of three buffers within the range of pH 1-8 at 37ºC (preferably pH 1.0, 4.6, 6.8) 49 50 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Solubility: Dose/solubility ratio and Do dose number D/S Gives the volume necessary to disolve the given dose of the active substance Dose Do ⎛D ⎞ Do = ⎜ 250 ⎟ ⎜ Cs ⎟ ⎝ ⎠ Drug solubility High solubility ensures that solubility is not likely to limit the dissolution and therefore absorption. 51 52 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 13
- 14. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Solubility: Dose/solubility ratio and Do dose number D/Sb 53 54 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV 55 56 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 14
- 15. Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV Dissolution rate: Dn dissolution number Solubility mg/mL Residence time Diffusivity in small intestine 5*10-6 cm2/s ~180 min ⎛ 3 D ⎞ ⎛ Cs ⎞ T ⋅ (Tres ) = res Dn = ⎜ ⋅ 2⎟⎜ρ ⎟ ⎝r ⎠ ⎝ ⎠ Tdiss Density Particle radius ~1.2mg/mL Time required for ~25μm Complete dissolution Rapid dissolution ensures that in vivo dissolution is not likely to be the rate limiting step 57 58 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica Estudios Liberación Estudios Liberación Tecnología Farmacéutica curso 2003-2004 Tecnología Farmacéutica curso 2003-2004 Correlaciones IVIV Correlaciones IVIV EMEA/CPMP and FDA/BCS Exemption criteria of IN VIVO studies High solubility, pH 1-7.5 High solubility, pH 1-8 (6.8) UE-EMEA USA-FDA (6.8) Linear and complete Rapid dissolution: Rapidly dissolving High permeability absorption (Fabs>90%) − Demonstrate similarity of − When no less than the 85% Rapid dissolution Rapid dissolution dissolution profile between of the labeled amount of the (T85<30min, test and reference in each of drug substance dissolves (T85<30min, pH=1.2,4.5,6.8) three buffers within the within 30 mins using USP pH=1.0,4.6,6.8) Excipients currently range of pH 1-8 at 37ºC apparatus I (100 rpm) or II Excipients well established approved for IR Dosage (preferably pH 1.0, 4.6, 6.8). (50 rpm) in a volume of 900 (not large doses) Forms (FDA Inactive mL or less in each of the − In cases where more than Ingredients List) Excluded drug with risks of following media 0.1 N HCL, 85% of the active substance Non-Narrow Therapeutic therapeutic failures (or SGF without enzymes) are dissolved within 15 Index drugs pH4.5 buffer, pH 6.8 buffer minutes, the similarity of or SIF (without enzymes). dissolution profiles may be accepted as demonstrated. 59 60 © © Prof. Marival Bermejo Prof. Marival Bermejo Depto. Farmacia y Tecnología Farmacéutica Depto. Farmacia y Tecnología Farmacéutica 15
