Tipos de reacciones químicas
•Descargar como PPT, PDF•
0 recomendaciones•3,046 vistas
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Organica 1 practica 3 ensayo de muestras preliminares

Organica 1 practica 3 ensayo de muestras preliminares
Solubilidad y conductividad eléctrica de las sales

Solubilidad y conductividad eléctrica de las sales
Similar a Tipos de reacciones químicas
Similar a Tipos de reacciones químicas (20)
Más de Videoconferencias UTPL
Más de Videoconferencias UTPL (20)
Asesoria trabajo fin de titulacion (Lineas y proyectos de investigación )

Asesoria trabajo fin de titulacion (Lineas y proyectos de investigación )
Asesoria trabajo fin de titulacion (objetivos y planificacion)

Asesoria trabajo fin de titulacion (objetivos y planificacion)
Tipos de reacciones químicas
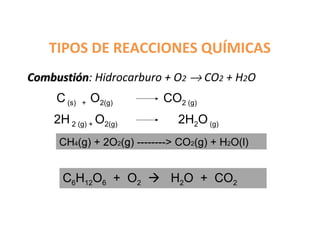
- 1. TIPOS DE REACCIONES QUÍMICAS Combustión: Hidrocarburo + O2 → CO2 + H2O Combustión C (s) + O2(g) CO2 (g) 2H 2 (g) + O2(g) 2H2O (g) CH4(g) + 2O2(g) --------> CO2(g) + H2O(l) C6H12O6 + O2 H2O + CO2
- 2. TIPOS DE REACCIONES QUÍMICAS Síntesis: A + B → C Síntesis 2Na (s) + Cl2 (g) 2 NaCl (s) +
- 3. TIPOS DE REACCIONES QUÍMICAS Descomposición: AB → A + B 2H2O (l) 2H2 (g) + O (g)
- 4. TIPOS DE REACCIONES QUÍMICAS Mg (s) + Cu2SO4 (s) MgSO4(s) + Cu (s) + + Sustitución Doble: AB + CD → AD + CB Doble 2NaOH (ac) + CuCl2 (ac) 2NaCl(ac) + Cu(OH)2 (s) Identifique…………………
- 6. RAZONES MOLARES Paso 1: escriba la reacción utilizando símbolos químicos. Paso 2: ajuste la ecuación química. 2 NO + 1 O2 → 2 NO2
- 7. CÁLCULOS DE MOL A MOL ¿Cuántos moles de H2O se producen cuando se queman 2,72 moles de H2 en un exceso de O2? 2 H2 + O2 → 2 H 2O Utilice el factor estequiométrico o la relación de moles en una ecuación: 2 mol H2O 2,72 mol H2 × = 2,72 mol H 2O 2 mol H2
- 8. CONVERSIONES MOL - GRAMO Para convertir en moles (n) los gramos (m) de cualquier sustancia sólo hay que dividir por la masa molecular (M) de dicha sustancia: ¿Cuántos moles hay en 24.5 g de (H2SO4)? Ya sabemos que el peso molecular es de 98 g/mol: Rta= 0.25 mol de H2SO4
- 9. GRACIAS 9
Notas del editor
- utpl
