Espectro
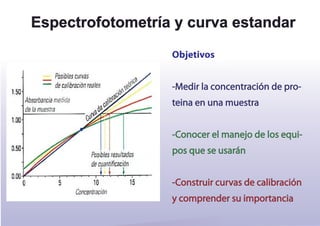
- 1. Espectrofotometría y curva estandar Objetivos -Medir la concentración de pro- teina en una muestra -Conocer el manejo de los equi- pos que se usarán -Construir curvas de calibración y comprender su importancia
- 2. Utilizamos los métodos espectrofotométri- cos para medir la concentración de proteína(s) en una muestra problema Según la región del espectro absorbida, puede ser: -Visible (colorimetría) -UV (ultravioleta)
- 3. ESPECTROFOTÓMETRO Color Longitud de onda(nm) Violeta 380-430 Azul 430-500 Cian 500-520 Verde 520-565 Amarillo 565-590 Naranja 590-625 Rojo 590-740
- 4. Ley de Beer & Lambert Establece que la absorbancia es proporcional al número de moléculas absorbentes A = ε·c·l A = absobancia c= concentración C l=longitud de la celda ε= coeficiente de extinción o absortividad molar
- 5. Coeficiente de extinción o absortividad molar Es una propiedad intrínseca de los compuestos. Es una medida de absorción de las sustancias a una determinada longitud de onda Unidades: ε[=]M-1cm-1 F o Phe 260nm W o Trp 295 nm Y o Tir 275nm
- 7. Determinación de la concentración de proteína Métodos para determinar la concentración de proteína en una muestra problema -Absorbancia a 280 nm -Reacción del Biuret - Método de Lowry - Método de Bradford
- 8. Método de absorbancia a 280nm -Absorción de los residuos de tirosilo y triptofanilo -Se lee a 280nm -Sensibilidad: 0.05-2.0mg(prot)/ml -Método no destructivo.
- 9. Método Biuret -Formación del complejo (violeta-prupura) Cu-Proteína ----------> -Condiciónes alcalinas -Se lee a 540 nm -Sensibilidad: 1.0-6.0 mg(prot)/ml.
- 10. Método Lowry --El complejo proteína-Cu (reacción de Biuret) se hace reaccionar con el reactivo de Folin-Ciocalteu o -Reducción del ácido fosfomolíbdico/fosfotúngstico (incrementa la intensidad del color azul) -Se lee a 750 nm -Sensibilidad: 0.1-2.0 ug(prot)/ml
- 11. Método Bradford -Unión del colorante azul de Coomasie a proteína -Condiciones de reacción fuertemente ácidas -Se lee a 595nm -Sensibilidad: 1.0-10.0 ug (prot)/ml
- 12. Método Ventajas Desventajas Alta especificidad por proteínas Biuret Poco sensible Pocas interferencias Barato Distintas proteínas reaccionan Mayor sensibilidad que diferente Lowry Biuret Interferencia con sulfato de amonio Bradford Muy sensible Interferencia con detergentes Directo Interferencia con ácidos nucléicos A 280nm No se pierde la muestra t1/2 (lámpara UV) 1000h/hombre
- 13. Curva Patrón Es un gráfico que permite conocer la cantidad de proteí- na en muestras problema a partir de concentraciones co- nocidas de proteína, utilizan- do la ecuación de la recta o interpolando las absorban- cias obtenidas
- 14. Determinación de proteínas por absor- bancia a 280 ηm 1. Rotular los tubos de microfuga 2. Añadir los volúmenes del estándar de BSA que se indican en la tabla y completar con agua. 3. Encender el espectrofotómetro por lo menos 15 minutos antes de la determinación y seleccionar la λ de 280 ηm. 4. Utilizar celda de cuarzo para realizar las mediciones. 5. Ajustar el espectrofotómetro a cero con agua. 6. Realizar las lecturas. 7. Llenar la tabla con los datos de absorbancia. 8. Calcular la concentración de proteína de acuerdo al volumen añadido de la solución estándar.
