Equilibrio Iónico y Ácidos Débiles
•Descargar como PPTX, PDF•
0 recomendaciones•842 vistas
equilibrio ionico
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (18)
Bioquimica de las proteinas y aminoacido (bioq. i)

Bioquimica de las proteinas y aminoacido (bioq. i)
Destacado (18)
Analisisinstrumentalfelipedejesshernndezbastar 110413025235-phpapp01

Analisisinstrumentalfelipedejesshernndezbastar 110413025235-phpapp01
Último
Último (16)
271706433-Horacio-Baliero-Casa-en-Punta-Piedras.pptx

271706433-Horacio-Baliero-Casa-en-Punta-Piedras.pptx
Arribando a la concreción II. Títulos en inglés, alemán y español

Arribando a la concreción II. Títulos en inglés, alemán y español
presentacion-auditoria-administrativa-i-encuentro (1).ppt

presentacion-auditoria-administrativa-i-encuentro (1).ppt
CERTIFICADO para NIÑOS, presentacion de niños en la iglesia .pptx

CERTIFICADO para NIÑOS, presentacion de niños en la iglesia .pptx
Unitario - Serie Fotográfica - Emmanuel Toloza Pineda

Unitario - Serie Fotográfica - Emmanuel Toloza Pineda
BIOGRAFIA MARIANO MELGAR presentacion en power point

BIOGRAFIA MARIANO MELGAR presentacion en power point
SEMIOLOGIA DE CABEZA Y CUELLO. Medicina Semiologia cabeza y cuellopptx

SEMIOLOGIA DE CABEZA Y CUELLO. Medicina Semiologia cabeza y cuellopptx
Europa y la Exploración del continente americano.pptx

Europa y la Exploración del continente americano.pptx
Equilibrio Iónico y Ácidos Débiles
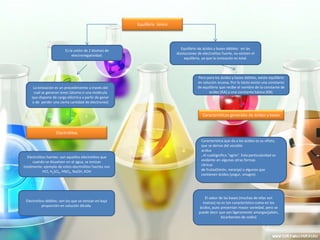
- 1. Equilibrio Iónico Es la unión de 2 átomos de electronegatividad. La ionización es un procedimiento a través del cual se generan iones (átomo o una molécula que dispone de carga eléctrica a partir de ganar o de perder una cierta cantidad de electrones) Equilibrio de ácidos y bases débiles: en las disoluciones de electrolitos fuerte, no existen el equilibrio, ya que la ionización es total. Pero para los ácidos y bases débiles, existe equilibrio en solución acuosa. Por lo tanto existe una constante de equilibrio que recibe el nombre de la constante de acidez (KA) y una constante básica (KB). Características generales de ácidos y bases Característica que da a los ácidos es su olfato, que se deriva del vocablo acidus , el cualsignifica "agrio". Esta particularidad es evidente en algunas otras formas cítricas de frutas(limón, naranja) o algunos que contienen ácidos (yogur, vinagre). El sabor de las bases (muchas de ellas son toxicas) no es tan característico como en los ácidos, pues presentan mayor variedad, pero se puede decir que son ligeramente amargas(jabón, bicarbonato de sodio) Electrolitos Electrolitos fuertes: son aquellos electrolitos que cuando se disuelven en el agua, se ionizan totalmente: ejemplo de estos electrolitos fuertes son HCl, H2SO4, HNO3, NaOH, KOH Electrolitos débiles: son los que se ionizan en baja proporción en solución diluida.