ENLACE QUÍMICO
•
1 recomendación•200 vistas
Conceptos básicos: estructura de lewis, formación de iones, enlace químico y sus tipos
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Recordemos las clases y el concepto del enlace quimico

Recordemos las clases y el concepto del enlace quimico
Similar a ENLACE QUÍMICO
Similar a ENLACE QUÍMICO (20)
Más de Belèn Cañizares
Más de Belèn Cañizares (8)
Último
El 7 de junio de 1890, por ejemplo, Henry Marmaduke Harris obtuvo una patente británica (Nº 8816) para "Máquinas aéreas con aerostatos" en las que el "coche... en forma de barco" estaba unido a un globo y era "impulsado por la reacción de los gases descargados a través de una boquilla... cuya dirección estaba controlada, relacionada con algún tipo de dispositivo o tecnología de dirección. ".1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...

1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...Champs Elysee Roldan
Último (20)
1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...

1890 –7 de junio - Henry Marmaduke Harris obtuvo una patente británica (Nº 88...
Althusser, Louis. - Ideología y aparatos ideológicos de Estado [ocr] [2003].pdf![Althusser, Louis. - Ideología y aparatos ideológicos de Estado [ocr] [2003].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Althusser, Louis. - Ideología y aparatos ideológicos de Estado [ocr] [2003].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Althusser, Louis. - Ideología y aparatos ideológicos de Estado [ocr] [2003].pdf
IAAS- EPIDEMIOLOGIA. antisepcsia, desinfección, epp

IAAS- EPIDEMIOLOGIA. antisepcsia, desinfección, epp
Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf![Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf
Moda colonial de 1810 donde podemos ver las distintas prendas

Moda colonial de 1810 donde podemos ver las distintas prendas
Ensayo ENRICH (sesión clínica, Servicio de Neurología HUCA)

Ensayo ENRICH (sesión clínica, Servicio de Neurología HUCA)
Perfiles NEUROPSI Atención y Memoria 6 a 85 Años (AyM).pdf

Perfiles NEUROPSI Atención y Memoria 6 a 85 Años (AyM).pdf
Flores Galindo, A. - La ciudad sumergida. Aristocracia y plebe en Lima, 1760-...

Flores Galindo, A. - La ciudad sumergida. Aristocracia y plebe en Lima, 1760-...
Glaeser, E. - El triunfo de las ciudades [2011].pdf![Glaeser, E. - El triunfo de las ciudades [2011].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Glaeser, E. - El triunfo de las ciudades [2011].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Glaeser, E. - El triunfo de las ciudades [2011].pdf
ENLACE QUÍMICO
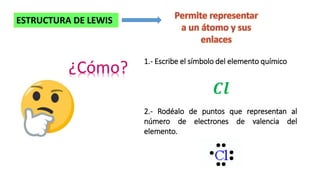
- 1. ESTRUCTURA DE LEWIS ¿Cómo? 1.- Escribe el símbolo del elemento químico 2.- Rodéalo de puntos que representan al número de electrones de valencia del elemento. 𝑪𝒍
- 2. 3.- Para representar una molécula, colocamos los electrones del enlace entre los átomos que lo forman:
- 3. REGLA DEL OCTETO Es la tendencia que tienen los átomos a adquirir ocho electrones en el último nivel de energía¿Por qué? Porque necesitan ganar estabilidad, adquiriendo una configuración electrónica lo más parecida al gas noble más cercano (el de su mismo período), sin embargo existen excepciones El análisis de las configuraciones electrónicas de los gases nobles muestran que, a excepción del helio, los gases nobles tienen ocho electrones en su nivel más externo.
- 5. FORMACIÓN DE IONES Es un átomo con carga positiva o negativa Los elementos más electronegativos tienden a ganar electrones de valencia Los elementos menos electronegativos y más electropositivos tienden a perder electrones de valencia
- 6. A un ion se lo representa mediante el símbolo de su elemento, con un superíndice a la derecha que indica la carga que posee mediante un numero y el signo + o el signo -. ANIÓN CLORUROCATIÓN CALCIO
- 7. LOS METALES con pocos electrones de valencia, ceden electrones Se convierten en LOS NO METALES con muchos electrones de valencia, reciben electrones Se convierten en Átomos cargados positivamente Átomos cargados negativamente
- 8. QUÍMICA ENLACE QUÍMICO - Fuerza que une de manera estable a los átomos, los iones o las moleculas que forman las sustancias quimicas (elementos y compuestos). - En laformacion deun enlace, los atomos tienden aceder, ganar o compartir electrones hasta que el numero deestos sea iguala ocho en su nivel de valencia. ≠ ESTRUCTURA ATÓMICA Enlace iónico Enlace covalente Enlace simple Enlace doble Enlace triple
- 9. ENLACE IÓNICO El enlace iónico es la unión resultante de la presencia de fuerzas electrostáticas entre iones positivos y negativos para dar lugar a la formación de un compuesto
- 10. ENLACE COVALENTE Consisten en la unión de dos átomos que comparten uno o mas pares de electrones.
- 11. TIPOS DE ENLACES COVALENTES SIMPLE Los dos átomos comparten un par de electrones. Por ejemplo, las moléculas de H2, Cl2 y H2O DOBLE Los átomos enlazados comparten dos pares de electrones. Por ejemplo, las moléculas de O2 y CO2. TRIPLE Los átomos enlazados comparten tres pares de electrones. Por ejemplo, las moléculas de N2 y C2H2 (etino).