Quimica2º1ª1ºClase8.pdf
•
0 recomendaciones•2 vistas
El documento explica la estructura electrónica, que es la distribución de electrones en niveles y orbitales energéticos de un átomo. Se proporcionan ejemplos de la estructura electrónica de varios elementos como oxígeno, flúor, aluminio y argón. Además, se indica que a partir del potasio, los primeros electrones se encuentran debajo del número de período y los últimos en el casillero correspondiente, dando ejemplos de potasio, hierro, yodo y plomo. Finalmente, se pide esc
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Más contenido relacionado
Similar a Quimica2º1ª1ºClase8.pdf
Similar a Quimica2º1ª1ºClase8.pdf (20)
ppt-quimica-nm8-configuracion-electronica-y-organizacion-de-la-tabla-periodic...

ppt-quimica-nm8-configuracion-electronica-y-organizacion-de-la-tabla-periodic...
La tabla periódica - Bloques - Propiedades periódicas

La tabla periódica - Bloques - Propiedades periódicas
Atomoejerciciosresueltos3eso 150222103305-conversion-gate02

Atomoejerciciosresueltos3eso 150222103305-conversion-gate02
Atomoejerciciosresueltos3eso 150222103305-conversion-gate02

Atomoejerciciosresueltos3eso 150222103305-conversion-gate02
Más de hjgeo
Más de hjgeo (15)
El protocolo de kyoto sobre el cambio climático está en vigor en la argentina

El protocolo de kyoto sobre el cambio climático está en vigor en la argentina
Diseño curricular tecnico en equipos e instalaciones electromecánica 1

Diseño curricular tecnico en equipos e instalaciones electromecánica 1
TECNICO EN EQUIPOS E INSTALACIONES ELECTROMECÁNICA Programa quimica3°2015

TECNICO EN EQUIPOS E INSTALACIONES ELECTROMECÁNICA Programa quimica3°2015
Último
Último (20)
🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
Prueba libre de Geografía para obtención título Bachillerato - 2024

Prueba libre de Geografía para obtención título Bachillerato - 2024
Análisis de los Factores Externos de la Organización.

Análisis de los Factores Externos de la Organización.
Tema 10. Dinámica y funciones de la Atmosfera 2024

Tema 10. Dinámica y funciones de la Atmosfera 2024
EL HABITO DEL AHORRO en tu idea emprendedora22-04-24.pptx

EL HABITO DEL AHORRO en tu idea emprendedora22-04-24.pptx
Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO

Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO
La Sostenibilidad Corporativa. Administración Ambiental

La Sostenibilidad Corporativa. Administración Ambiental
TALLER DE DEMOCRACIA Y GOBIERNO ESCOLAR-COMPETENCIAS N°3.docx

TALLER DE DEMOCRACIA Y GOBIERNO ESCOLAR-COMPETENCIAS N°3.docx
Quimica2º1ª1ºClase8.pdf
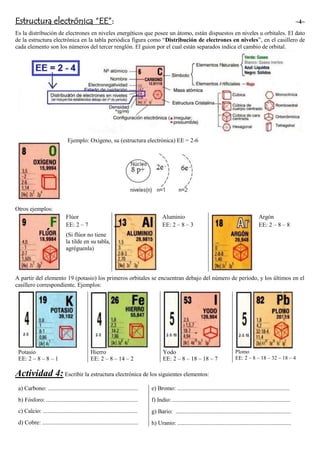
- 1. Estructura electrónica “EE”: ~4~ Es la distribución de electrones en niveles energéticos que posee un átomo, están dispuestos en niveles u orbitales. El dato de la estructura electrónica en la tabla periódica figura como “Distribución de electrones en niveles”, en el casillero de cada elemento son los números del tercer renglón. El guion por el cual están separados indica el cambio de orbital. Ejemplo: Oxígeno, su (estructura electrónica) EE = 2-6 Otros ejemplos: Flúor EE: 2 – 7 (Si flúor no tiene la tilde en su tabla, agréguenla) Aluminio EE: 2 – 8 – 3 Argón EE: 2 – 8 – 8 A partir del elemento 19 (potasio) los primeros orbitales se encuentran debajo del número de período, y los últimos en el casillero correspondiente. Ejemplos: Potasio EE: 2 – 8 – 8 – 1 Hierro EE: 2 – 8 – 14 – 2 Yodo EE: 2 – 8 – 18 – 18 – 7 Plomo EE: 2 – 8 – 18 – 32 – 18 – 4 Actividad 4: Escribir la estructura electrónica de los siguientes elementos: a) Carbono: ............................................................. b) Fósforo: .............................................................. c) Calcio: ................................................................ d) Cobre: ................................................................. e) Bromo: ............................................................................ f) Indio: ................................................................................ g) Bario: .............................................................................. h) Uranio: .............................................................................