Corrosion cuadro y resultados
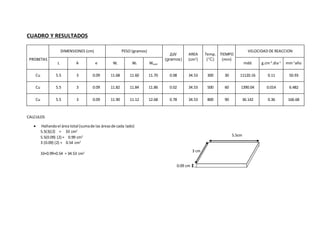
- 1. CUADRO Y RESULTADOS CALCULOS Hallandoel área total (sumade las áreasde cada lado) 5.5(3)(2) = 33 cm2 5.5(0.09) (2) = 0.99 cm2 3 (0.09) (2) = 0.54 cm2 33+0.99+0.54 = 34.53 cm2 PROBETAS DIMENSIONES (cm) PESO (gramos) ΔW (gramos) AREA (cm2 ) Temp. (°C) TIEMPO (min) VELOCIDAD DE REACCION L A e Wi Wf Woxid mdd g.cm-2 .dia-1 mm-1 año Cu 5.5 3 0.09 11.68 11.60 11.70 0.08 34.53 300 30 11120.16 0.11 50.93 Cu 5.5 3 0.09 11.82 11.84 11.86 0.02 34.53 500 60 1390.04 0.014 6.482 Cu 5.5 3 0.09 11.90 11.12 12.68 0.78 34.53 800 90 36.142 0.36 166.68 5.5cm 3 cm 0.09 cm
- 2. Velocidadde reacción:mdd(mgdm-2 dia-1 ) 0.08𝑔 (34.53 𝑐𝑚2)(30min) 𝑥 (10𝑐𝑚)2 (1𝑑𝑚)2 60𝑚𝑖𝑛 1ℎ 24ℎ 1𝑑𝑖𝑎 1000𝑚𝑔 1𝑔 = 11120.76 𝑚𝑔 𝑑𝑚−2 𝑑𝑖𝑎−1 0.02𝑔 (34.53 𝑐𝑚2)(60min) ∗ (10𝑐𝑚)2 (1𝑑𝑚)2 ∗ 60𝑚𝑖𝑛 1ℎ ∗ 24ℎ 1𝑑𝑖𝑎 ∗ 1000𝑚𝑔 1𝑔 = 1390.09 𝑚𝑔 𝑑𝑚−2 𝑑𝑖𝑎−1 0.78𝑔 (34.53 𝑐𝑚2)(90min) ∗ (10𝑐𝑚)2 (1𝑑𝑚)2 ∗ 60𝑚𝑖𝑛 1ℎ ∗ 24ℎ 1𝑑𝑖𝑎 ∗ 1000𝑚𝑔 1𝑔 = 36142.48 𝑚𝑔 𝑑𝑚−2 𝑑𝑖𝑎−1 Velocidadde reacción(gcm-2 dia-1 ) 0.08𝑔 (34.53 𝑐𝑚2)(30min) ∗ 60𝑚𝑖𝑛 1ℎ 24ℎ 1𝑑𝑖𝑎 = 0.11𝑔 𝑐𝑚−2 𝑑𝑖𝑎−1 0.02𝑔 (34.53 𝑐𝑚2)(60min) ∗ 60𝑚𝑖𝑛 1ℎ 24ℎ 1𝑑𝑖𝑎 = 0.014𝑔 𝑐𝑚−2 𝑑𝑖𝑎−1 0.78𝑔 (34.53 𝑐𝑚2)(90min) ∗ 60𝑚𝑖𝑛 1ℎ 24ℎ 1𝑑𝑖𝑎 = 0.36𝑔 𝑐𝑚−2 𝑑𝑖𝑎−1 Velocidadde reacción(mmaño-1 ) 𝑔. 𝑚−2 𝑑𝑖𝑎−1 = 0.0463 𝑚𝑚.𝑎ñ𝑜−1 1. 1 𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 463 𝑚𝑚. 𝑎ñ𝑜−1 0.11𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 𝑋 = 50.93𝑚𝑚. 𝑎ñ𝑜−1 2. 1 𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 463 𝑚𝑚. 𝑎ñ𝑜−1 0.014𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 𝑋 = 6.482𝑚𝑚. 𝑎ñ𝑜−1 3. 1 𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 463 𝑚𝑚. 𝑎ñ𝑜−1 0.36𝑔. 𝑐𝑚−2 𝑑𝑖𝑎−1 → 𝑋 = 166.68𝑚𝑚. 𝑎ñ𝑜−1 RESULTADOS Se oxidó el óxido cobre en un horno de mufla en intervalo de temperatura de 300 a 800 C °. El incremento de peso durante la oxidación se determinó usando una balanza de precisión El tiempo de oxidación se determinó de forma tal, que la ganancia de peso correspondiese a la del peso estequiométrico para la formación del óxido cuproso. Una vez que el cobre fue completamente oxidado, las muestras oxidadas fueron enfriadas a temperatura ambiente y retiradas de la balanza para ser pesadas y medidas Al aumentar la temperatura del horno, el peso ganado por la oxidación también se incrementa, teniendo un mayor peso ganado cuando el cobre se oxida a 800°C.
- 3. A simple vista se revela la presencia de un oxido poroso que permite la difusión del oxígeno en la superficie del cobre. La difusión de oxigeno se ve reflejada cuando observamos el incremento de peso del cobre bajo diferentes temperaturas de trabajo. La resistencia del cobre a la corrosión es menor a la de otros materiales, tal es el caso de latón, donde se pudo evidenciar la facilidad con el que el cobre se oxidaba a la menor temperatura del ensayo. BIBLIOGRAFIA MeijeringJ.L.,Verheijke M.L.(1959), “Oxidationkineticsinthe case of ageingoxide films”,ActaMetall,7, 331 p. www.textoscientificos.com/Quimica/corrosion
