Formulación de ácido nitroso y ácido pirohipoantimonioso
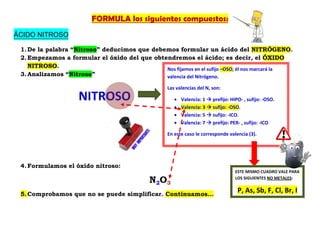
- 1. FORMULA los siguientes compuestos: ÁCIDO NITROSO 1. De la palabra “Nitroso” deducimos que debemos formular un ácido del NITRÓGENO. 2. Empezamos a formular el óxido del que obtendremos el ácido; es decir, el ÓXIDO NITROSO. Nos fijamos en el sufijo –OSO; él nos marcará la 3. Analizamos “Nitroso” valencia del Nitrógeno. Las valencias del N, son: NITROSO • Valencia: 1 prefijo: HIPO- , sufijo: -OSO. • Valencia: 3 sufijo: -OSO. • Valencia: 5 sufijo: -ICO. • Valencia: 7 prefijo: PER- , sufijo: -ICO En este caso le corresponde valencia (3). 4. Formulamos el óxido nitroso: ESTE MISMO CUADRO VALE PARA N2O3 LOS SIGUIENTES NO METALES: 5. Comprobamos que no se puede simplificar. Continuamos… P, As, Sb, F, Cl, Br, I
- 2. 6. Una vez que tenemos la fórmula simplificada del óxido, el siguiente paso es añadirle agua. 7. En el caso del nitrógeno solo le añadiremos una molécula de agua, ya que no pertenece al grupo de los elementos no metálicos polihidroxilados (P, As, Sb, B, Si). 8. Procedemos: N2O3 + H2O H2N2O4 9. Por último, simplificamos la fórmula del ácido obtenida: H2N2O4 HNO2
- 3. ÁCIDO PIROHIPOANTIMONIOSO PIROHIPO HIPOANTIMONIOSO Se trata del Antimonio, uno de los no metales a los que se 1. En este caso primero vamos a analizar el nombre: les pueden añadir varias moléculas de agua (1,2 o 3) PIROHIPOANTIMONIOSO PIROHIPOANTIMONIOSO HIPO El prefijo PIRO indica que Nos fijamos en el afijo HIPO y en el sufijo –OSO; nos marcarán la tendremos que añadir dos valencia del Antimonio. moléculas de agua al óxido; ya que se trata de un Las valencias del Sb, son: elemento • Valencia: 1 prefijo: HIPO- , sufijo: -OSO. “polihidroxilado”, el • Valencia: 3 sufijo: -OSO. Antimonio. Recordamos: • Valencia: 5 sufijo: -ICO. • META 1 H2O • Valencia: 7 prefijo: PER- , sufijo: -ICO • PIRO 2 H2O En este caso le corresponde valencia (1). • ORTO* 3 H2O (*) el ORTO se puede omitir
- 4. 2. Empezamos formulando el óxido del que obtendremos el ácido; es decir, el ÓXIDO HIPOANTIMONIOSO. Sabemos que la valencia del Sb, es (1), según el cuadro anterior. Sb2O1 3. Comprobamos que no se puede simplificar. Continuamos… 4. Una vez que tenemos la fórmula simplificada del óxido, el siguiente paso es añadirle agua. 5. En el caso del Sb le añadiremos dos moléculas de agua, ya que SI, pertenece al grupo de los elementos no metálicos polihidroxilados (P, As, Sb, B, Si). Le añadimos dos moléculas de agua porque aparece el prefijo PIRO en el nombre (ver cuadro). 6. Procedemos: Sb2O + 2H2O H4Sb2O3 7. Por último, comprobamos que no se puede simplificar.