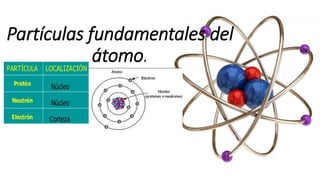
Partículas fundamentales del átomo
- 2. Electrón (e-) • Son extremadamente pequeños y muy livianos. Es fácil retirar electrones de los átomos y usarlos excitados como fuente de electricidad y en aparatos como televisores, computadores, etc. • También se pueden usar en su modalidad ionizada como por ejemplo en los Rayos X. • Posee una masa de 9,1x10-28 g (es 1.836 veces más liviano que el Protón) y una carga eléctrica relativa de -1 • Fue descubierto por el Físico Británico J.J. Thomson en 1897, quién publica su trabajo en 1905. • Se considera que es un Leptón ya que no estaría constituido por otras sub-partículas (como los Quarks)
- 3. Protón • • Los científicos pensaban originalmente que no existía nada más pequeño que el Protón en el núcleo del átomo. • • Lo descubre Ernest Rutherford • • Su masa es 1,67x10-24 g • • Se representa como P+ y tiene una carga eléctrica positiva • • Su masa es 1.837 veces mayor que la del electrón
- 4. Quarks • • En 1968 los científicos descubrieron nuevas partículas dentro del Protón. Las llamaron Quarks. • • Hay tres quarks en cada protón y los quarks se mantienen unidos mediante otras partículas llamadas Gluones, que no tienen masa ni carga eléctrica; sólo poseen energía electromagnética
- 5. Neutrón • El Neutrón fue identificado por primera vez en 1932 por el físico británico James Chadwick. • No tiene carga eléctrica • Está conformado por la unión de un Protón, un Electrón (se anulan sus cargas eléctricas) y un Neutrino • Poseen una masa prácticamente igual a la del protón
- 6. Quarks • En 1968 los científicos descubrieron nuevas partículas dentro del Neutrón. Estas tres partículas también eran quarks, unidas también por energía electromagnética llamadas Gluones
- 7. Nomenclatura Atómica • Los elementos suelen indicarse mediante una abreviatura alfabética que recibe el nombre de símbolo numérico • X = Símbolo químico del elemento. • Z = Número atómico, es el número de protones en el núcleo. • A = Número de masa, es el número de nucleones (protones + neutrones). • Un núcleo representado de esta manera es también llamado un nucleído.
