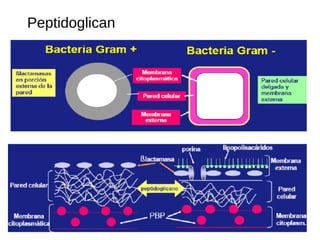
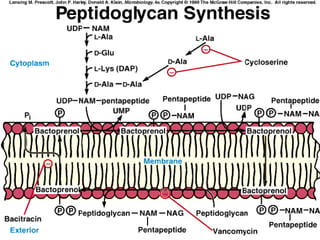
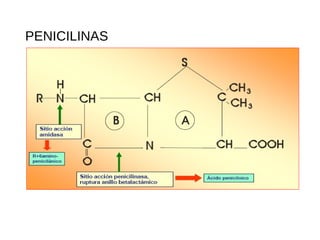
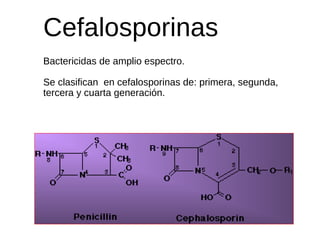
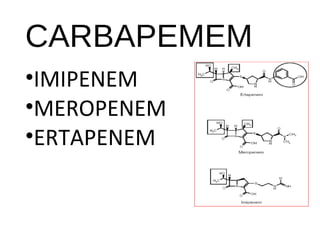
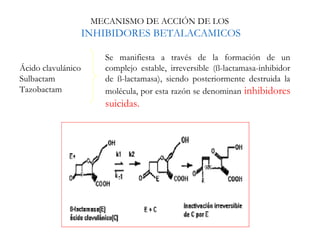
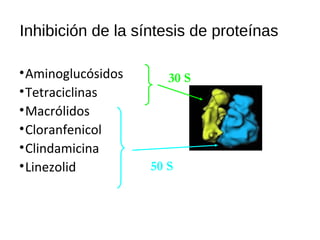
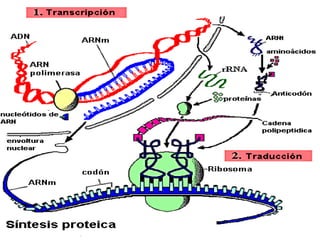
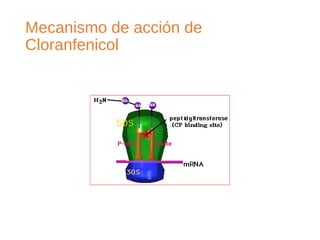
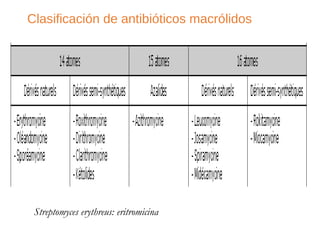
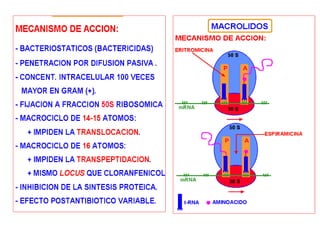
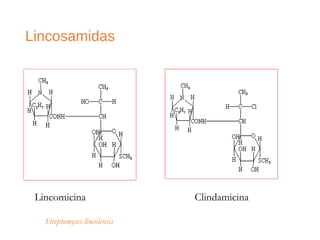
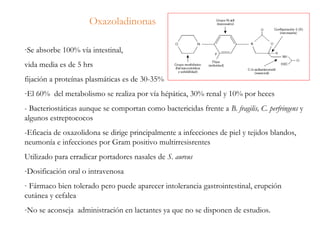
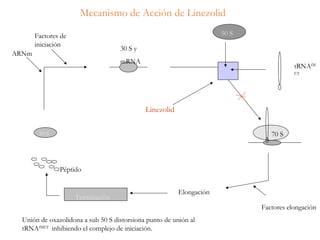
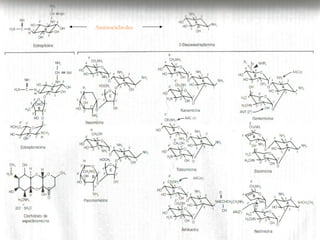
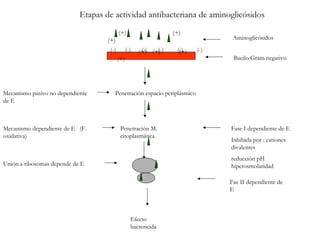
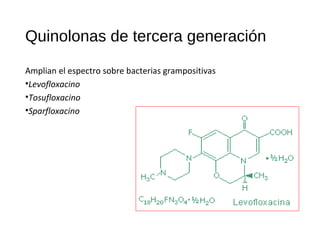
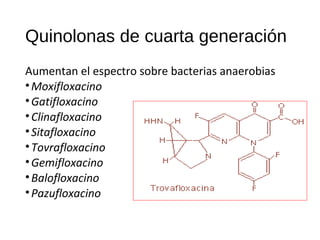
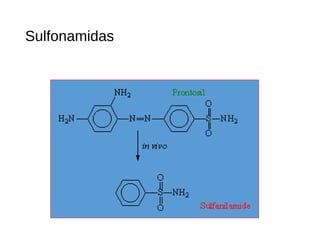
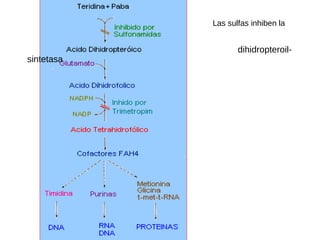
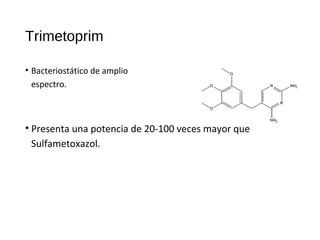
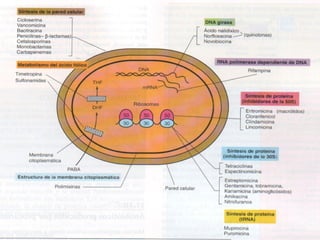
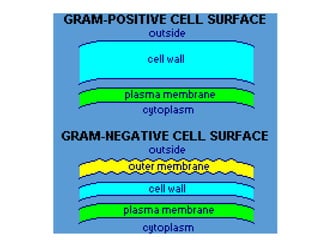
El documento clasifica y describe diferentes tipos de microorganismos y antibióticos. Describe la clasificación de bacterias según su morfología, tinción de Gram y metabolismo. Explica el mecanismo de acción y clasificación de diferentes antibióticos como penicilinas, cefalosporinas, carbapenemes, aminoglucósidos y tetraciclinas. También cubre conceptos como farmacocinética, farmacodinamia y mecanismos de resistencia a antibióticos.















![Farmacodinamia
ATB tiempo dependientes
CIM
[ ]
tiempo
• Beta lactámicos
• Macrólidos
• Clindamicina](https://image.slidesharecdn.com/antibioticos2-161102083920/85/Antibioticos-2-23-320.jpg)
![Farmacodinamia
ATB concentración dependientes
CIM
[ ]
tiempo
• Aminoglucósidos
• Quinolonas
• Metronidazol](https://image.slidesharecdn.com/antibioticos2-161102083920/85/Antibioticos-2-24-320.jpg)