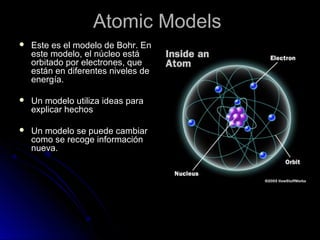
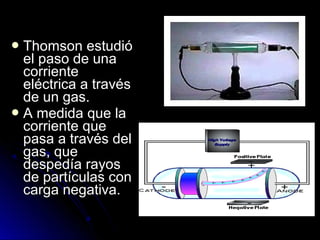
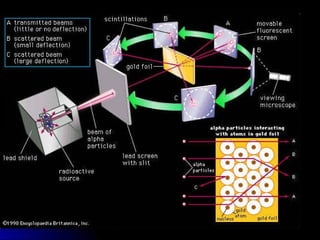
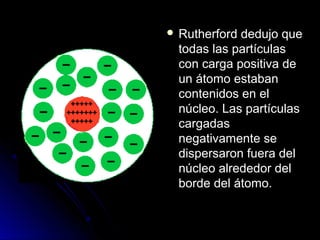
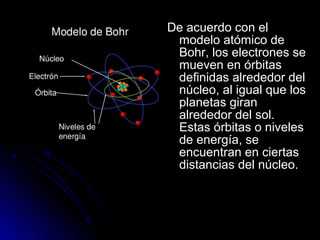
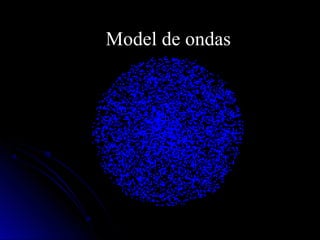
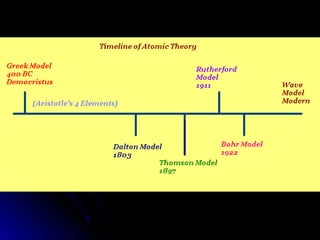
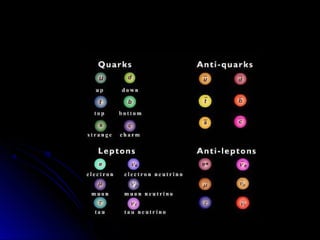
Este documento resume la historia de la teoría atómica desde Demócrito en el 400 AC hasta el modelo actual basado en la mecánica cuántica. Demócrito propuso la existencia de átomos indivisibles llamados "átomos", pero su teoría fue ignorada durante 2000 años. En el 1800, Dalton reintrodujo la idea de los átomos y propuso que los elementos químicos están compuestos de átomos únicos. Más tarde, experimentos mostraron que los átomos contenían partículas más pequeñas como electrones