Historia y proceso de la síntesis Haber-Bosch en la producción de amoniaco.pdf
•
0 recomendaciones•145 vistas
El proceso Haber-Bosch consiste en sintetizar amoniaco a partir de nitrógeno e hidrógeno a altas presiones y temperaturas. Fritz Haber desarrolló el proceso en 1909 y Bosch lo mejoró a escala industrial. La reacción clave es N2 + 3H2 → 2NH3, la cual se lleva a cabo en un convertidor a 200 atmósferas y 450-500°C. Este proceso es crucial para la producción industrial de amoniaco y fertilizantes nitrogenados.
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Autor: I. Q. Victor M. Alcerreca Sánchez
Fecha: 1991-03Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...

Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...Academia de Ingeniería de México
Más contenido relacionado
La actualidad más candente
Autor: I. Q. Victor M. Alcerreca Sánchez
Fecha: 1991-03Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...

Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...Academia de Ingeniería de México
La actualidad más candente (20)
67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan

67786760 ejercicios-resueltos-de-gases-ideales-y-gases-reales-roldan
Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...

Catálisis, su evolución desde la alquimia hasta su reconocimiento como disc...
Solucionario himmanblue 6edic mercadolibre.com.himmelblau

Solucionario himmanblue 6edic mercadolibre.com.himmelblau
Procesos Reversibles e irreversibles. Termodinámica

Procesos Reversibles e irreversibles. Termodinámica
Solucionario de balance Materia RODRIGO LONDOÑO GARCÍA

Solucionario de balance Materia RODRIGO LONDOÑO GARCÍA
Solucionario De Fenomenos De Transporte R Byron Bird

Solucionario De Fenomenos De Transporte R Byron Bird
Similar a Historia y proceso de la síntesis Haber-Bosch en la producción de amoniaco.pdf
Similar a Historia y proceso de la síntesis Haber-Bosch en la producción de amoniaco.pdf (20)
Informe iv-produccion-de-hidrogeno-a-partir-de-biogas-editado[1]![Informe iv-produccion-de-hidrogeno-a-partir-de-biogas-editado[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Informe iv-produccion-de-hidrogeno-a-partir-de-biogas-editado[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Informe iv-produccion-de-hidrogeno-a-partir-de-biogas-editado[1]
Último
Último (20)
APORTES A LA ARQUITECTURA DE WALTER GROPIUS Y FRANK LLOYD WRIGHT

APORTES A LA ARQUITECTURA DE WALTER GROPIUS Y FRANK LLOYD WRIGHT
Aportes a la Arquitectura de Le Corbusier y Mies Van der Rohe

Aportes a la Arquitectura de Le Corbusier y Mies Van der Rohe
INSUMOS QUIMICOS Y BIENES FISCALIZADOS POR LA SUNAT

INSUMOS QUIMICOS Y BIENES FISCALIZADOS POR LA SUNAT
Tippens fisica 7eDIAPOSITIVAS TIPENS Tippens_fisica_7e_diapositivas_33.ppt

Tippens fisica 7eDIAPOSITIVAS TIPENS Tippens_fisica_7e_diapositivas_33.ppt
CALCULO SISTEMA DE PUESTA A TIERRA PARA BAJA TENSION Y MEDIA TENSION

CALCULO SISTEMA DE PUESTA A TIERRA PARA BAJA TENSION Y MEDIA TENSION
LA APLICACIÓN DE LAS PROPIEDADES TEXTUALES A LOS TEXTOS.pdf

LA APLICACIÓN DE LAS PROPIEDADES TEXTUALES A LOS TEXTOS.pdf
NTP- Determinación de Cloruros en suelos y agregados (1) (1).pptx

NTP- Determinación de Cloruros en suelos y agregados (1) (1).pptx
Ficha Tecnica de Ladrillos de Tabique de diferentes modelos

Ficha Tecnica de Ladrillos de Tabique de diferentes modelos
Maquinaria Agricola utilizada en la produccion de Piña.pdf

Maquinaria Agricola utilizada en la produccion de Piña.pdf
Historia y proceso de la síntesis Haber-Bosch en la producción de amoniaco.pdf
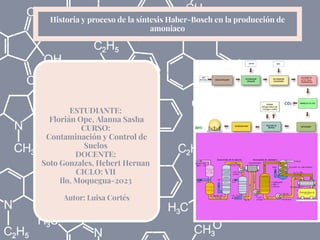
- 1. ESTUDIANTE: Florián Ope, Alanna Sasha CURSO: Contaminación y Control de Suelos DOCENTE: Soto Gonzales, Hebert Hernan CICLO: VII Ilo, Moquegua-2023 Historia y proceso de la síntesis Haber-Bosch en la producción de amoniaco Autor: Luisa Cortés
- 2. Síntesis Haber- Bosch Historia de la síntesis Haber-Bosch Partió del nitrógeno del aire a un ritmo de 100-125 ml por hora. Fue en 1909 cuando Fritz desarrolló un proceso para obtener amoniaco. Tuvo una enorme importancia estratégica durante la IGM. El proceso de Haber Bosch proporcionó al bando alemán una fuente abundante de amoniaco para la fabricación de explosivos. Este proceso tiene gran importancia a nivel industrial, ya que es el más usado para obtener amoniaco en grandes cantidades. El proceso de Haber-Bosch es la reacción de nitrógeno e hidrógeno gaseosos para producir amoniaco. La importancia de la reacción radica en la dificultad de producir amoniaco a un nivel industrial. Dio con la solución y Bosch ideó la manera de sintetizar amoniaco a gran escala. "En tiempo de paz, un cientifico pertenece al mundo, pero en tiempo de guerra pertenece a su país". F. Haber
- 3. proceso de la síntesis Haber- Bosch En resumen, el proceso de Haber-Bosch consiste en la sintesis de amoniaco a partir de nitrógeno e hidrógeno, en condiciones de elevada presión (200 atm) y elevada temperatura (450-500C). La reacción que tiene lugar es: N2(g) + 3H2(g) <-> 2NH3(g) En un reformador secundario se añade aire a la corriente gaseosa, produciendo la combustión del CH4 restante y consiguiendo el N2 necesario. PASO 6 PASO 5 En el reformador primario reaccionan CH4 y vapor de H2O para producir hidrógeno. CH4(g) + H2O(g) -> CO(g) + 2H2(g) El CO2 envenena al catalizador al momento de producir el amoniaco, se retira en las torres de extracción. PASO 1 PASO 2 PASO 3 PASO 4 La corriente gaseosa de H2 y N2 en una relación de 3 a 1 alimenta al convertidor, opera a una presión de 200 atm y 400- 500C. El amoniaco puede ser transportado a presión o alimentado a una planta mediante una tubería. El rendimiento de la reacción es de 15 al 20% en enfría a 10C el amoniaco se condensa y es retirado como líquido.