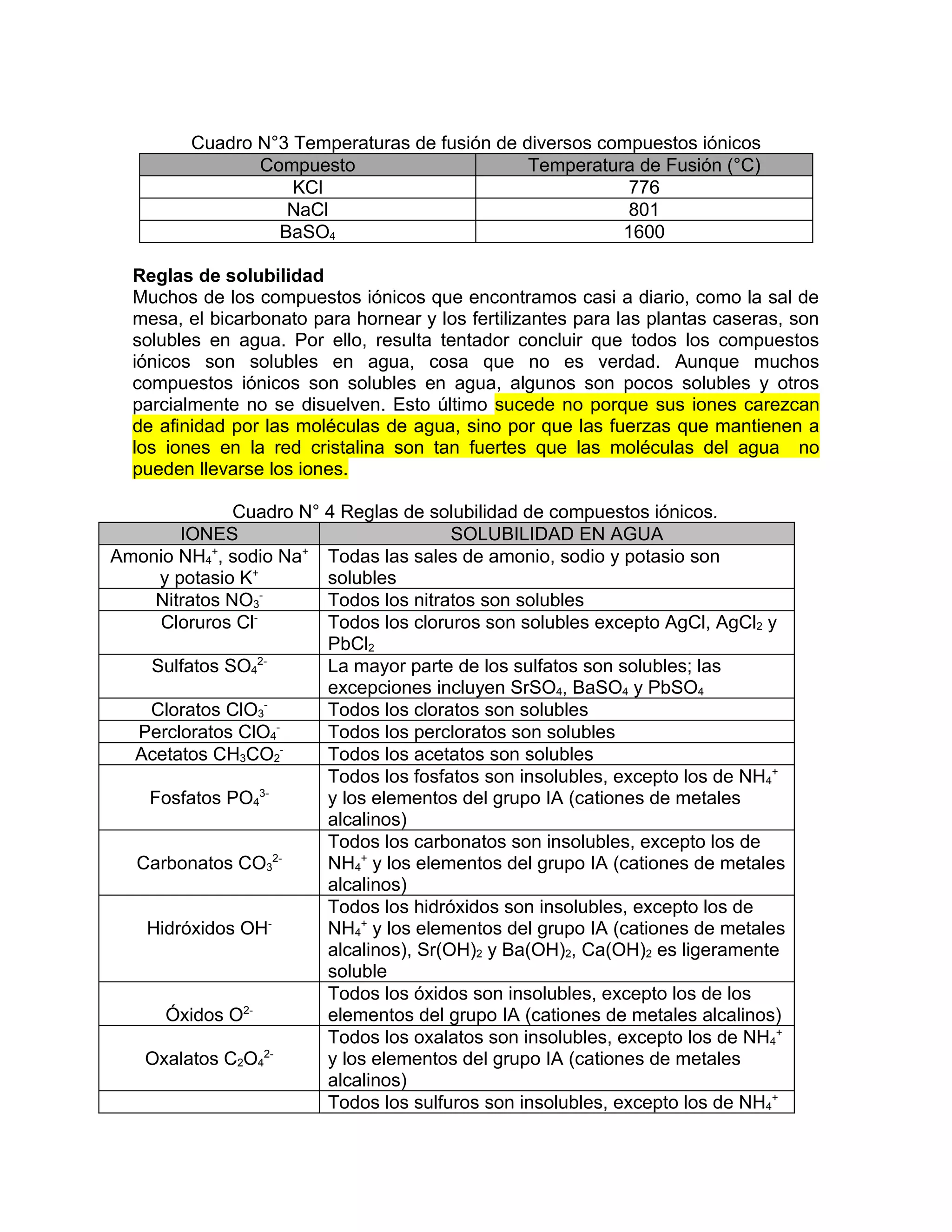
Las sales son compuestos iónicos formados por la combinación de un catión y un anión. Son sólidos cristalinos con altas temperaturas de fusión y ebullición. Muchas sales son solubles en agua, donde sus iones se separan y pueden conducir electricidad, haciéndolas electrolitos. Las propiedades de solubilidad de las sales dependen de los iones que las componen y se rigen por reglas generales de solubilidad.