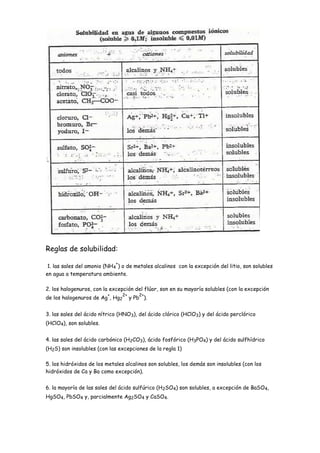
Las siguientes sustancias son generalmente solubles en agua: sales de los metales alcalinos como el sodio y el potasio, excepto las del litio; la mayoría de los haluros, excepto los de plata, mercurio y plomo; las sales de los ácidos nítrico, clórico y perclórico; la mayoría de las sales del ácido sulfúrico, excepto las de bario, mercurio, plomo y plata; e hidróxidos de los metales alcalinos. Las sales de los ácidos carbónico, fos