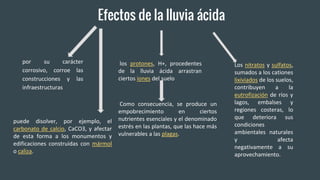
La lluvia ácida se forma cuando los óxidos de nitrógeno y azufre emitidos por fuentes como fábricas y vehículos se combinan con el agua en la atmósfera. Estos gases forman ácidos que caen a la tierra con la lluvia. La lluvia ácida corroe construcciones y disuelve minerales en el suelo, afectando a plantas y ecosistemas acuáticos. Algunas soluciones incluyen reducir las emisiones de estas fuentes de contaminación y agregar compuestos alcalinos a