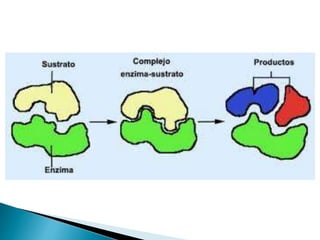
1. Las actividades químicas celulares son complejas y están catalizadas por enzimas.
2. Las enzimas son proteínas producidas por las células que actúan como catalizadores para acelerar reacciones químicas sin ser consumidas.
3. Diferentes factores como la concentración de enzimas y sustratos, el pH y la temperatura afectan la velocidad de las reacciones catalizadas por enzimas.