La nitración es un proceso químico para introducir un grupo nitro mediante la reacción entre un compuesto orgánico y un agente nitrante como el ácido nítrico. Es una de las reacciones químicas comercialmente más importantes y se usa para producir compuestos como nitrobenceno y nitrocelulosa. El mecanismo de nitración depende de los reactivos y condiciones e involucra reacciones iónicas o radicales libres.
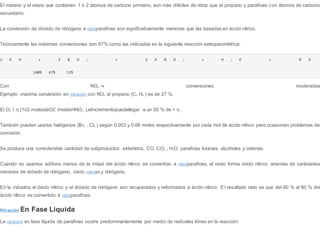
![Muchas nitraciones iónicas emplean ácidos mezcla, la que usualmente contiene ácido nítrico + un ácido fuerte, por ejemplo áci do sulfúrico / ácido
perclórico / ácido hidrofluórico / resinas de intercambio iónico conteniendo grupos de ácido sulfónico utilizan al agente nitrante en solución líquida.
En muchos casos se presentan 2 fases inmiscibles (líquidas) dentro del reactor, se mantiene una leve presión sobre la atmosférica para conservar las
dos fases líquidas. En la fase orgánica se concentran los nitrohidrocarburos. En la fase ácida se concentra el agua. El lugar de la nitración propiamente
dicha está junto a la interfase.
Por razones de seguridad la operación es :
a. A presión atmosférica
b. Rango de temperaturas [0 a 120] ºC por lo tanto el rendimiento será función de la temperatura = f (T)
Este tipo de nitración aumenta el tiempo de residencia (oscila alrededor de 1 hora). Además no se deben utilizar temperaturas menores a 0 ºC dado
que el rendimiento bajará y se incrementará el costo de refrigeración.
Agentes de nitración iónica
Frecuentemente se utiliza HNO3 (HO.NO2)
Por razones de viabilidad y economía la nitración a escala industrial se lleva a cabo habitualmente con una mezcla de ácidos nítrico y sulfúrico (mezcla
sulfonítrica), y de vez en cuando con ácido nítrico acuoso, ácido nítrico en ácido acético, o ácido nítrico en anhídrido acético. El uso de ácidos de
componentes alternativos, tales como ácido perclórico, ácido fluorhídrico, o trifluoruro de boro se limita a importantes estudios de soporte. Estos a
veces son llevadas a cabo en disolventes orgánicos inertes tales como hidrocarburos clorados o sulfolano para dar mezclas de reacción homogéneas.
La verdadera especie nitrante en reacciones tipo iónica es el nitronio NO2
+
El ácido nítrico puro, ionizado produce pequeñas cantidades de ión nitronio.](https://image.slidesharecdn.com/nitracion7-191014212822/85/Nitracion7-4-320.jpg)
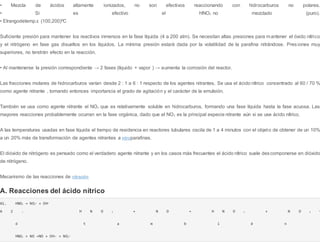
![La primera reacción es rápida y la segunda lenta.
La presencia de H2O (producida durante la nitración) disminuye la concentración del ión [NO2
+] (=> desplazamiento de la reacción hacia la izquierda).
La eficiencia de nitración es mayor usando ácido sulfúrico H2SO4 ú Oleum (SO3 + H2SO4)](https://image.slidesharecdn.com/nitracion7-191014212822/85/Nitracion7-5-320.jpg)

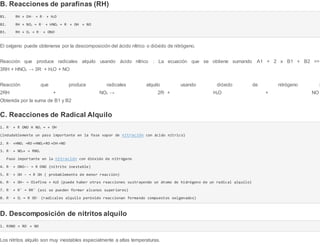
![agitador, también incide en la cinética. Gotas de tamaño muy pequeño, impulsados a altas velocidades disminuyen la transferencia de masa del
reactivo hacia la fase dispersa. La composición del ácido y las fases orgánicas afectan también la tensión superficial entre las fases. Esta relación
(ácido/fase orgánica) es importante por el tipo de emulsión que se forma y por el área entre fases.
Si la temperatura sube demasiado, el grado de exotermia de la reacción puede volverse fuera de control, produciéndose reaccio nes laterales ó
explosiones.
Se emplean reactores que están compartimentados en serie con un eficiente agitador en cada uno, tal el proceso para el TNT ó la Nitroglicerina.
Otros poseen un tubo principal y 2 laterales; la emulsión es reciclada muchas veces por el primero con grandes zonas de transferencia de calor.
La recirculación ocurre mediante una bomba en el fondo de cada tubo lateral, que a la vez provee la agitación y mezcla de los reactivos.
Desventajas
Ácido sulfúrico diluido
Concentración ácido para venta ó reuso ⇒ aumento del costo energía calórica
Costo de tratamiento para eliminar vestigios de materia orgánica.
Idem anterior p/restos nítrico y nitroso.
Nunca se consigue mejor calidad por altísimos costos. (Rango [ ] de 90 a 98 %)
Altos costos de instalaciones de tratamiento
Ventajas
Rol deshidratante del S O3 (remueve agua de reacción)
Promotor de la ionización HNO3 → NO2
+
( se comporta como catalizador)
Ventas del subproducto (auge minería, lixiviación)
Algunas nitraciones como C-Nitración son altamente irreversibles. La energía libre de Gibbs en nitración es grande y negativa.](https://image.slidesharecdn.com/nitracion7-191014212822/85/Nitracion7-8-320.jpg)

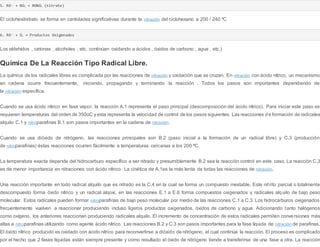
![Si el grupo es por ejemplo: —CF3
-
, los electrones se concentran en las posiciones meta y para.
Una vez hecha la 1o nitración (mono), resulta más dificil introducir el 2º grupo nitro(dinitración) y así progresivamente para la 3ª.
Condiciones muy severas, mayor temperatura y mayor riesgo. También requieren mayor [ácidos] ⇒ mayor [NO2
+
].
Se producen reacciones secundarias y subproductos di-trinitrados que se convierten en impurezas a eliminarlas por razones de seguridad en los
siguientes pasos.
Aromáticos como fenoles, éteres fenólicos, fáciles de nitrar, son nitrados con mezclas de ácidos nítricos y un plus mayor de ácido nitroso. La ionización
de esta mezcla produce el ión nitrosilo (NO+) como sigue:
HNO3 + HNO2 ⇌ NO+
+ NO3
+
+ H2O
El ión nitrosilo ataca al compuesto aromático
El aromático nitroso es oxidado con ácido nítrico formando nitroaromáticos y volviendo a formar ácido nitroso.
Ar NO + HNO3 → Ar NO2 + HNO2 (regeneración)
2- Nitración de Alcoholes](https://image.slidesharecdn.com/nitracion7-191014212822/85/Nitracion7-12-320.jpg)
![ Nitraciones en fase vapor
Nitraciones en fase líquida.
Nitración En Fase Vapor
Baja presión (para obtener mezclas gaseosas de hidrocarburos, agentes nitrantes, productos e inertes)
Cuando se usa HNO3 como agente nitrante el rango de temperaturas es de 350 a 450 ºC.
Cuando se usa dióxido de Nitrógeno → temperatura ∈ ( 200 a 450 ) ºC
En altas temperaturas la reacción es instantánea; a bajas temperaturas aumenta el tiempo de reacción para obtener un adecuado grado
de nitraciónllegando al orden de varios minutos.
Mayor exotermia, mayor temperatura ⇒ ↑↑ riesgo de explosividad ⇒ estricto control de temperaturas.
Los procedimientos comunes para el control de las temperaturas son :
a. Usar exceso de hidrocarburos, 4:1 con relación del hidrocarburo al agente nitrante; el cual actúa disminuyendo la temperatura.
b. Adición de un gas inerte (vapor, N2 ) a la mezcla que reacciona. A veces se usa ácido nítrico diluido (60%) formándose grandes cantidades de
vapor.
c. Diseño de una adecuada transferencia de calor, tubos de aluminio de diámetro pequeño en baño de sal fundida.
d. Reactores de lecho fluido también proveen un excelente control de temperatura.
e. Empleo del calor de reacción por vaporización, calefaccionando la alimentación de ácido nítrico usado como agente nitrante. este es
pulverizado dentro de un vapor propano caliente.
Las presiones varían entre [1 , 12] atm.
En nitraciones en fase vapor de parafinas usando ácido nítrico, resulta máxima la conversión de éste a varias nitroparafinas, desde cerca del 20 % en
el caso del metano a aprox. el 40 % para parafinas altas como el n-butano. El ácido nítrico residual se convierte en óxidos de nitrógeno
Las conversiones crecen conforme aumenta el peso molecular de las parafinas.](https://image.slidesharecdn.com/nitracion7-191014212822/85/Nitracion7-14-320.jpg)