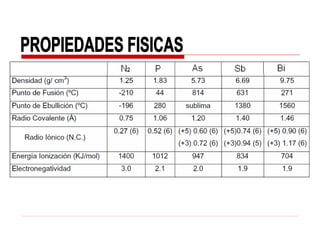
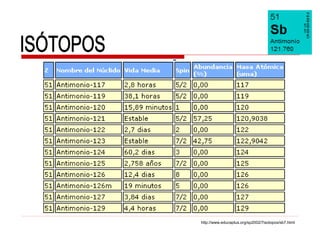
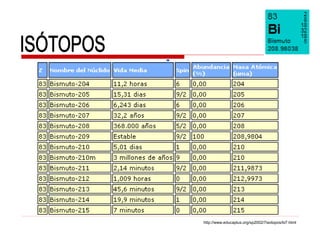
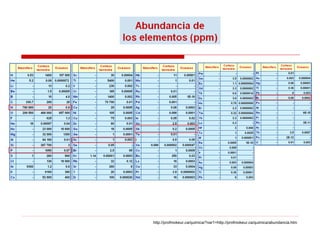
El documento describe las diferentes formas alotrópicas del fósforo y sus propiedades. El fósforo se presenta en varias formas alotrópicas, incluyendo fósforo blanco, rojo y negro. El fósforo blanco es una sustancia molecular compuesta de moléculas de P4 tetraédricas, mientras que el fósforo rojo es una forma cristalina y el fósforo negro es amorfo y pirolítico.
![Configuración electrónica: [GN] ns2np3](https://image.slidesharecdn.com/grupo15-121106122814-phpapp02/85/Grupo15-1-320.jpg)