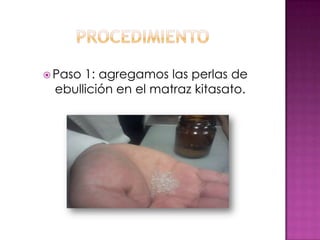
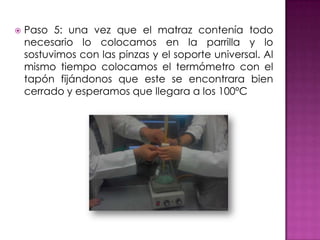
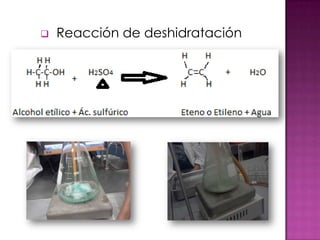
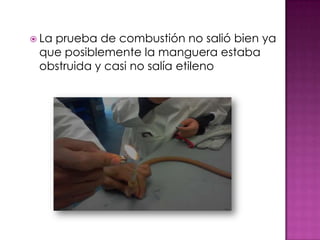
Este documento presenta un experimento de laboratorio para obtener etileno mediante una reacción de deshidratación entre alcohol etílico y ácido sulfúrico. Describe los materiales, procedimiento y pruebas realizadas para comprobar la producción de etileno, incluyendo reacciones de combustión, adición y oxidación. El objetivo era producir etileno y verificar su identidad a través de estas pruebas químicas.