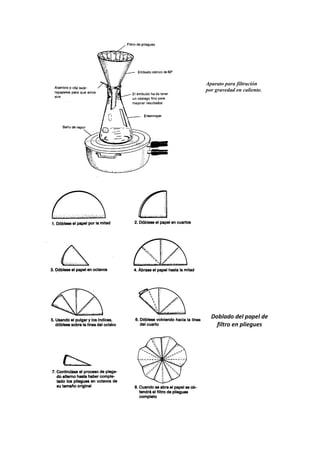
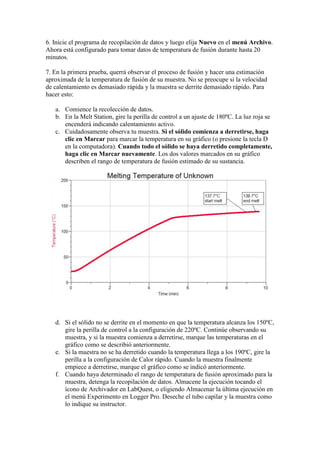
Este documento describe un procedimiento para aislar la trimiristina de la nuez moscada. Se realiza una extracción sólido-líquido usando n-hexano como solvente, seguida de una destilación simple para concentrar la solución. Luego se induce la cristalización de la trimiristina agregando metanol, y se determina el punto de fusión para verificar la pureza del producto aislado.