Preparacion de la Muestra
•Descargar como PPT, PDF•
8 recomendaciones•22,051 vistas
El documento describe las etapas básicas del proceso analítico químico, incluyendo la preparación de la muestra, la medición y transducción de la señal, y el tratamiento de datos. La preparación de la muestra es la etapa más importante, consumiendo alrededor del 60% del tiempo total del análisis y siendo responsable de la mayoría de los errores. Los objetivos de la preparación de la muestra son hacer el analito accesible para su detección y medida, obtenerlo a una concentración adecuada, y eliminar interferencias
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Practica-DETERMINACIÓN GRAVIMÉTRICA DE COBRE EN UNA SAL SOLUBLE

Cuantificar el contenido de cobre en una muestra de una sal soluble por precipitación del ion cúprico con una solución acuosa de hidróxido de potasio para formar el hidróxido de cobre que por calentamiento de la solución provocaremos la oxidación para obtener oxido de cobre (CuO).
Practica 8 (preparacion y estandarizacion del edta)

Química Analítica y Métodos Instrumentales
Equipo numero 1
Universidad Veracruzana
Ing. Química 302
Cuaderno de problemas de cinética química y catálisis

El cuaderno contiene, un conjunto de fundamentos al inicio de cada tema, en los que se presentan las bases teóricas que dan sustento a la solución matemática presentada en los problemas resueltos. Los fundamentos teóricos no incluyen un análisis profundo de la deducción matemática usada para llegar a las ecuaciones presentadas, pues estas son debidamente presentadas en clase, y el uso del cuaderno pretende ser un apoyo a la clase impartida por el profesor, no sustituirla por completo.
Finalmente, se presenta un conjunto de problemas propuestos para que el alumno desarrolle la habilidad adquirida durante la clase y de la lectura y análisis de los problemas aquí resueltos. Además, para que el alumno pueda comparar con sus resultados de acuerdo a su procedimiento, se anexa también el resultado correcto de los problemas propuestos.
Recomendados
Practica-DETERMINACIÓN GRAVIMÉTRICA DE COBRE EN UNA SAL SOLUBLE

Cuantificar el contenido de cobre en una muestra de una sal soluble por precipitación del ion cúprico con una solución acuosa de hidróxido de potasio para formar el hidróxido de cobre que por calentamiento de la solución provocaremos la oxidación para obtener oxido de cobre (CuO).
Practica 8 (preparacion y estandarizacion del edta)

Química Analítica y Métodos Instrumentales
Equipo numero 1
Universidad Veracruzana
Ing. Química 302
Cuaderno de problemas de cinética química y catálisis

El cuaderno contiene, un conjunto de fundamentos al inicio de cada tema, en los que se presentan las bases teóricas que dan sustento a la solución matemática presentada en los problemas resueltos. Los fundamentos teóricos no incluyen un análisis profundo de la deducción matemática usada para llegar a las ecuaciones presentadas, pues estas son debidamente presentadas en clase, y el uso del cuaderno pretende ser un apoyo a la clase impartida por el profesor, no sustituirla por completo.
Finalmente, se presenta un conjunto de problemas propuestos para que el alumno desarrolle la habilidad adquirida durante la clase y de la lectura y análisis de los problemas aquí resueltos. Además, para que el alumno pueda comparar con sus resultados de acuerdo a su procedimiento, se anexa también el resultado correcto de los problemas propuestos.
Volumetría de neutralización - Método Directo y por Retroceso del Ácido sulfú...

Informe Escrito de la Titulación Directa y por Retroceso del ácido sulfúrico. En el anexo se encuentra el link del videotutorial que acompaña el trabajo.
Métodos Volumetricos de Análisis

En esta presentación se incluye una descripcióny los calculos asociados a los métodos volumétricos de análisis existentes.
DETERMINACION ÁCIDO FOSFORICO EN REFRESCOS DE COLA

LABORATORIO DE DETERMINACIÓN DE ÁCIDO FOSFÓRICO EN REFRESCOS DE COLA
Test de Dixon (Test – Q). Rev. 00

Hay ocasiones cuando se realiza una serie de análisis de réplicas, es posible que el conjunto de datos contenga uno (o posiblemente más) datos cuestionable o no coherente con los restantes, es decir, que difiera notablemente y de forma inexplicable de los otros, incluso que parezca estar fuera del intervalo de los errores aleatorios que podrían ser producidos por el procedimiento. Por desgracia, no hay criterios uniformes que se puedan usar para decidir si un dato atípico se pueda atribuir a un error accidental más que a una variación casual.
Preparación y valoración de soluciones

El presente informe busca:
Conocer las técnicas básicas para la preparación de soluciones de distintas concentraciones físicas y químicas.
Valorar una solución ácida y determinar su concentración.
Valorar una solución básica y determinar su concentración.
Más contenido relacionado
La actualidad más candente
Volumetría de neutralización - Método Directo y por Retroceso del Ácido sulfú...

Informe Escrito de la Titulación Directa y por Retroceso del ácido sulfúrico. En el anexo se encuentra el link del videotutorial que acompaña el trabajo.
Métodos Volumetricos de Análisis

En esta presentación se incluye una descripcióny los calculos asociados a los métodos volumétricos de análisis existentes.
DETERMINACION ÁCIDO FOSFORICO EN REFRESCOS DE COLA

LABORATORIO DE DETERMINACIÓN DE ÁCIDO FOSFÓRICO EN REFRESCOS DE COLA
Test de Dixon (Test – Q). Rev. 00

Hay ocasiones cuando se realiza una serie de análisis de réplicas, es posible que el conjunto de datos contenga uno (o posiblemente más) datos cuestionable o no coherente con los restantes, es decir, que difiera notablemente y de forma inexplicable de los otros, incluso que parezca estar fuera del intervalo de los errores aleatorios que podrían ser producidos por el procedimiento. Por desgracia, no hay criterios uniformes que se puedan usar para decidir si un dato atípico se pueda atribuir a un error accidental más que a una variación casual.
Preparación y valoración de soluciones

El presente informe busca:
Conocer las técnicas básicas para la preparación de soluciones de distintas concentraciones físicas y químicas.
Valorar una solución ácida y determinar su concentración.
Valorar una solución básica y determinar su concentración.
La actualidad más candente (20)
Volumetría de neutralización - Método Directo y por Retroceso del Ácido sulfú...

Volumetría de neutralización - Método Directo y por Retroceso del Ácido sulfú...
Métodos analíticos. Unidad 1 análisis instrumental 1

Métodos analíticos. Unidad 1 análisis instrumental 1
DETERMINACION ÁCIDO FOSFORICO EN REFRESCOS DE COLA

DETERMINACION ÁCIDO FOSFORICO EN REFRESCOS DE COLA
Práctica 9. Determinación de dureza total y dureza de calcio

Práctica 9. Determinación de dureza total y dureza de calcio
Determinación de la acidez en leche beatriz afán de rivera

Determinación de la acidez en leche beatriz afán de rivera
Similar a Preparacion de la Muestra
Química analítica

“ La Química analítica es una ciencia metrológica que desarrolla, optimiza y aplica herramientas de amplia naturaleza,
Presentación de Bioquímica y Toxicología

En esta presentación podrás observar la medición de efectos a nivel de transcripción
Control del Proceso en la Disolucion de la Muetsra por VH

Curso dictado en el Hotel el Condado por LMS consulting
Similar a Preparacion de la Muestra (20)
Modulo 9 PREPARACIÓN DE MUESTRAS 11-convertido.pptx

Modulo 9 PREPARACIÓN DE MUESTRAS 11-convertido.pptx
Control del Proceso en la Disolucion de la Muetsra por VH

Control del Proceso en la Disolucion de la Muetsra por VH
Preparacion de la Muestra
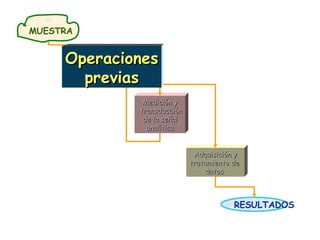
- 1. RESULTADOS Medición y transducción de la señal analítica Adquisición y tratamiento de datos ETAPAS BÁSICAS DEL PROCESO ANALÍTICO Operaciones previas Operaciones previas MUESTRA
- 2. Muestra bruta Muestreo Preservación Disolución Disgregación Instrumento Medición masa-volumen Pulverización tamizado Homogeneización Secado Reacciones analíticas Destrucción materia orgánica Técnicas separativas Otras reacciones químicas Transporte introducción instrumento
- 3. MATRIZ MUESTRAS Inorgánica Biológica Orgánica MUESTRA Sólidas Gaseosas Líquidas
- 4. CONCENTRACIÓN ANALITOS Macrocomponentes Trazas Microcomponentes ANALITOS Inorgánicos Orgánicos Bioquímicos
- 5. Participación humana Lentitud Fuente de errores Complejidad Peligrosidad Difícil control OPERACIONES PREVIAS Ampliamente variables
- 6. PREPARACIÓN DE LA MUESTRA Etapas de un Análisis Químico OPERACIONES PREVIAS
- 7. PREPARACIÓN DE LA MUESTRA 61% TRATAMIENTO DE DATOS 27% ANÁLISIS 6% ADQUISICIÓN DE DATOS 6% DISTRIBUCIÓN DE TIEMPO EN EL PROCESO ANALITICO
- 8. DISTRIBUCIÓN DE ERRORES GENERADOS DURANTE EL ANÁLISIS DE LA MUESTRA
- 9. MUY IMPORTANTE 6O,6% MODERADAMENTE IMPORTANTE 31% NO IMPORTANTE 1,6% MINIMAMENTE IMPORTANTE 6,8% IMPORTANCIA DE LA PREPARACIÓN DE LA MUESTRA
- 11. PREPARACIÓN DE LA MUESTRA 1. Llevar un porcentaje de analitos tan alto como sea posible desde la muestra original al paso de determinación 2. Obtener los analitos en el estado de agregación más adecuado para el procedimiento instrumental a utilizar, asegurando que los analitos permanecen en su estado original ó están totalmente convertidos en una especie estable. 3. Llevar sólo algunos de los componentes de la matriz de la muestra original al paso de determinación. 4. Obtener el analito a una concentración apropiada para la detección y medida. 5. No añadir ninguna nueva interferencia.
- 14. concentración de analito obtenido en el ensayo concentración de analito en la muestra % de RECUPERACIÓN = 100 x peso de analito obtenido en el ensayo peso de analito en la muestra % de RECUPERACIÓN = 100 x Estas pérdidas impiden una transferencia cuantitativa del material, que se expresa como PORCENTAJE DE RECUPERACIÓN
- 16. TÉCNICAS SEPARATIVAS Muestra A A Muestra A B C D E B C D E A TS TS B E D C A TS