PRESION EN LOS GASES.ppt
•Descargar como PPT, PDF•
0 recomendaciones•13 vistas
El documento describe los componentes principales del aire seco, incluidos el nitrógeno (78%), el oxígeno (21%) y el argón (0.93%). También cubre las leyes de los gases, como las leyes de Boyle, Charles y Avogadro, y la ecuación del gas ideal.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Cap. ii. comport. del gas nat. 1(1 49)

Este documento describe las propiedades y comportamiento del gas natural. Explica que el gas natural está compuesto principalmente por metano y cantidades menores de otros hidrocarburos como etano y propano. También cubre las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Avogadro, y cómo estas leyes se combinan en la ecuación general de los gases ideales. Finalmente, discute cómo calcular la densidad, volumen específico y gravedad específica de los gases ideales usando esta ecuación.
Clase 1 repaso de conocimientos previos

Este documento describe un curso de fisicoquímica que incluye: 1) clases teóricas semanales de 3 horas y clases de consulta, 2) exámenes y otros eventos de evaluación, 3) libros de texto recomendados. El curso cubre temas como las leyes del equilibrio, la transmisión de calor, los fenómenos de fase relacionados con la hidrología y las emisiones gaseosas. El objetivo es comprender los procesos físicos y químicos para predecirlos y controlarlos
Aire Julio 31 Julio[1]![Aire Julio 31 Julio[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Aire Julio 31 Julio[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
El documento describe la estructura y composición de la atmósfera terrestre. Se divide en cuatro capas principales: troposfera, estratosfera, mesosfera e ionosfera. La troposfera es donde ocurren los fenómenos meteorológicos y contiene el 99% del aire que respiramos. La estratosfera contiene la capa de ozono que nos protege de la radiación ultravioleta. El aire se compone principalmente de nitrógeno (78%) y oxígeno (21%), además de pequeñas
Gases

CONCEPTO ,CARACTERISTICAS , LEYES DE LOS GASES , UN BREVE RESEÑA SOBRE BOYLE , AVOGRADO,DALTON,CHARLES
Semana 1 gases ideal ambiental

Este documento presenta las leyes fundamentales de los gases. En primer lugar, se describe el estado gaseoso y las propiedades de compresibilidad y baja densidad de los gases. Luego, se explican la ley de Avogadro, las leyes de Boyle y Mariotte, y las leyes de Charles sobre la relación entre volumen, presión y temperatura de los gases. Finalmente, se introduce la ecuación general de los gases ideales.
Leyes gases2

Este documento describe las propiedades y leyes de los gases. Explica que los gases están compuestos de partículas que se mueven libremente y que la presión que ejercen los gases se debe a los choques de las partículas con las paredes del recipiente. Resume las leyes de Boyle, Charles y Avogadro, indicando que la presión y el volumen de los gases varían inversamente, directamente con la temperatura y directamente con la cantidad de sustancia, respectivamente.
Leyes gases

Este documento resume las principales leyes de los gases. Explica que la ley de Avogadro establece que a presión y temperatura constantes, volúmenes iguales de gases contienen el mismo número de moléculas. La ley de Boyle dice que a temperatura y cantidad de materia constantes, el volumen de un gas es inversamente proporcional a la presión. Finalmente, la ley de Charles establece que a presión y cantidad de materia constantes, el volumen de un gas es directamente proporcional a la temperatura absoluta.
Leyes fundamentales de los gases

Este documento presenta las leyes fundamentales de los gases y la teoría cinética de los gases. Explica brevemente el estado gaseoso, las medidas en gases y resume las leyes de Avogadro, Boyle y Mariotte, y Charles y Gay-Lussac. También describe la ecuación general de los gases ideales y el modelo molecular que explica estas leyes en términos del movimiento y colisiones de las partículas que componen los gases.
Recomendados
Cap. ii. comport. del gas nat. 1(1 49)

Este documento describe las propiedades y comportamiento del gas natural. Explica que el gas natural está compuesto principalmente por metano y cantidades menores de otros hidrocarburos como etano y propano. También cubre las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Avogadro, y cómo estas leyes se combinan en la ecuación general de los gases ideales. Finalmente, discute cómo calcular la densidad, volumen específico y gravedad específica de los gases ideales usando esta ecuación.
Clase 1 repaso de conocimientos previos

Este documento describe un curso de fisicoquímica que incluye: 1) clases teóricas semanales de 3 horas y clases de consulta, 2) exámenes y otros eventos de evaluación, 3) libros de texto recomendados. El curso cubre temas como las leyes del equilibrio, la transmisión de calor, los fenómenos de fase relacionados con la hidrología y las emisiones gaseosas. El objetivo es comprender los procesos físicos y químicos para predecirlos y controlarlos
Aire Julio 31 Julio[1]![Aire Julio 31 Julio[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Aire Julio 31 Julio[1]](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
El documento describe la estructura y composición de la atmósfera terrestre. Se divide en cuatro capas principales: troposfera, estratosfera, mesosfera e ionosfera. La troposfera es donde ocurren los fenómenos meteorológicos y contiene el 99% del aire que respiramos. La estratosfera contiene la capa de ozono que nos protege de la radiación ultravioleta. El aire se compone principalmente de nitrógeno (78%) y oxígeno (21%), además de pequeñas
Gases

CONCEPTO ,CARACTERISTICAS , LEYES DE LOS GASES , UN BREVE RESEÑA SOBRE BOYLE , AVOGRADO,DALTON,CHARLES
Semana 1 gases ideal ambiental

Este documento presenta las leyes fundamentales de los gases. En primer lugar, se describe el estado gaseoso y las propiedades de compresibilidad y baja densidad de los gases. Luego, se explican la ley de Avogadro, las leyes de Boyle y Mariotte, y las leyes de Charles sobre la relación entre volumen, presión y temperatura de los gases. Finalmente, se introduce la ecuación general de los gases ideales.
Leyes gases2

Este documento describe las propiedades y leyes de los gases. Explica que los gases están compuestos de partículas que se mueven libremente y que la presión que ejercen los gases se debe a los choques de las partículas con las paredes del recipiente. Resume las leyes de Boyle, Charles y Avogadro, indicando que la presión y el volumen de los gases varían inversamente, directamente con la temperatura y directamente con la cantidad de sustancia, respectivamente.
Leyes gases

Este documento resume las principales leyes de los gases. Explica que la ley de Avogadro establece que a presión y temperatura constantes, volúmenes iguales de gases contienen el mismo número de moléculas. La ley de Boyle dice que a temperatura y cantidad de materia constantes, el volumen de un gas es inversamente proporcional a la presión. Finalmente, la ley de Charles establece que a presión y cantidad de materia constantes, el volumen de un gas es directamente proporcional a la temperatura absoluta.
Leyes fundamentales de los gases

Este documento presenta las leyes fundamentales de los gases y la teoría cinética de los gases. Explica brevemente el estado gaseoso, las medidas en gases y resume las leyes de Avogadro, Boyle y Mariotte, y Charles y Gay-Lussac. También describe la ecuación general de los gases ideales y el modelo molecular que explica estas leyes en términos del movimiento y colisiones de las partículas que componen los gases.
Tfb03 gases i

El documento describe las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Gay-Lussac. Explica que un gas ideal se compone de moléculas perfectamente elásticas que interactúan débilmente. Las leyes relacionan la presión, volumen y temperatura de un gas, y son importantes para entender las propiedades de los gases y su comportamiento.
Estado gaseoso

1) La ecuación NaN3(s) → Na(s) + N2(g) representa la descomposición del azida sódico en sodio sólido y nitrógeno gaseoso.
2) El documento fue compilado por Alexánder Gutiérrez M. y Roberto Gutiérrez P. como parte de su programa de licenciatura en biología y química.
3) Se proporciona información sobre los diferentes estados de la materia, propiedades de los gases, leyes de los gases y teoría cinética molecular.
Estado gaseoso

El documento describe la descomposición del azida de sodio en sodio metálico y nitrógeno gaseoso. Explica que el azida de sodio se descompone en sodio sólido y nitrógeno gaseoso. También incluye los nombres de los autores que compilaron la información.
ESTADOGASPPT

El documento describe las propiedades de los gases y la teoría cinética molecular. Según la teoría, los gases están compuestos de partículas en constante movimiento que se mueven libremente y chocan entre sí. Las propiedades de los gases, como su expansibilidad y compresibilidad, se deben a la gran distancia entre las moléculas. La teoría también explica cómo las variables de estado como la presión, el volumen y la temperatura están relacionadas a través de las leyes de los gases ideales.
presentacionleyesdelosgases-100114093741-phpapp02.pptx

Este documento presenta las leyes fundamentales de los gases y la teoría cinética molecular. Explica las leyes de Avogadro, Boyle y Mariotte, y Charles y Gay-Lussac, así como la ecuación general de los gases ideales. También describe el modelo molecular que explica estas leyes en términos del movimiento y las colisiones de las partículas que componen los gases. Finalmente, incluye un apéndice sobre recursos educativos relacionados con las leyes de los gases.
04 Gases 21 03 05

El documento resume las principales leyes de los gases, incluyendo la ley de Boyle, la ley de Charles, la ley de Avogadro y la ley de los gases ideales. Explica que la presión y el volumen de los gases están inversamente relacionados a temperatura constante según la ley de Boyle, y que el volumen de los gases es directamente proporcional a la temperatura a presión constante según la ley de Charles. También cubre conceptos como el volumen molar y la densidad de los gases.
Cap 1 gases

1) La termodinámica estudia las propiedades de los gases, las leyes de los gases ideales y reales, y el equilibrio químico.
2) La teoría cinético molecular explica el comportamiento de los gases usando un modelo en el que las moléculas se mueven rápidamente y se golpean entre sí y las paredes del contenedor.
3) Las ecuaciones de estado relacionan variables de estado como la presión, volumen y temperatura para describir el comportamiento de los gases. La ecuación del gas ideal es una aproximación pero
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...CristianQuispeCerron
El documento presenta las propiedades empíricas de los gases, incluyendo las leyes de Boyle, Charles, Gay-Lussac y Avogadro. Explica la ecuación de estado de los gases ideales y cómo se relacionan el volumen, la presión, la temperatura y la cantidad de sustancia. También cubre conceptos como la constante de los gases, la distribución barométrica y ejercicios prácticos sobre la aplicación de estas leyes.Diapositivas gases

El documento describe la composición de la atmósfera terrestre y los gases que contiene además del nitrógeno y oxígeno mayoritarios. Explica las propiedades de los gases y las leyes que rigen su comportamiento, incluyendo las leyes de Boyle, Charles y Gay-Lussac, así como la teoría cinética de los gases y el concepto de gases ideales.
Leyes gases 1

Este documento resume las leyes fundamentales de los gases ideales y reales. Explica que un gas se define por su volumen, presión, temperatura y cantidad de sustancia. A continuación, describe las leyes de Avogadro, Boyle, Charles y Gay-Lussac, y la ecuación general de los gases ideales PV=nRT. También cubre el comportamiento real de los gases mediante la ecuación de Van der Waals y la ley de Dalton de las presiones parciales.
Fiqui estado gaseoso

El documento describe los conceptos fundamentales del estado gaseoso y el modelo del gas ideal. Explica las leyes de Boyle, Charles y Gay-Lussac, y la ecuación de estado del gas ideal. También cubre temas como mezclas de gases, humedad en el aire, y desviaciones del comportamiento ideal observadas en gases reales.
Física (II Bimestre)

Universidad Técnica Particular de Loja
Gestión Ambiental
Física
II Bimestre
Abril-Agosto 2007
Ponente: Mg. Henry Quezada
Leyes De Los Gases

El documento describe las leyes de los gases, incluyendo la Ley de Boyle, la Ley de Charles y la Ley de Gay-Lussac. Explica que la presión y el volumen de un gas varían inversamente a temperatura constante según la Ley de Boyle, y varían directamente con la temperatura a presión o volumen constante según las Leyes de Charles y Gay-Lussac, respectivamente.
Tema 2

1) El documento describe las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Gay-Lussac, y la ley combinada de los gases. 2) Explica cómo estas leyes se pueden usar para derivar la ecuación de estado de los gases ideales. 3) También cubre conceptos como presión parcial, volumen molar y densidad de los gases.
Laboratorio de gases ideales

Este documento presenta información sobre los gases ideales, incluyendo sus estados, leyes y fórmulas. Explica las leyes de Boyle, Charles, Gay-Lussac y la ley generalizada de los gases, además de realizar ejercicios prácticos aplicando estas leyes. El objetivo es ayudar a los estudiantes a comprender mejor los conceptos fundamentales relacionados con los gases ideales.
Teoria de los gases ideales comportamiento

Este documento describe las propiedades de los gases ideales y reales. Los gases ideales se comportan de manera ideal a presiones bajas y altas temperaturas, mientras que los gases reales se comportan de manera no ideal a presiones altas y bajas temperaturas. También explica las leyes de Boyle, Charles y Avogadro, y presenta la ecuación de estado de los gases ideales.
Las leyes de los gases.

El documento resume las principales leyes de los gases. La ley de Boyle establece que a temperatura constante, el volumen de un gas es inversamente proporcional a la presión. La ley de Charles establece que a presión constante, el volumen de un gas es directamente proporcional a la temperatura absoluta. La ley de Gay-Lussac establece que a volumen constante, la presión de un gas es directamente proporcional a la temperatura absoluta. Las tres leyes se combinan en la ecuación general de los gases ideales, donde la presión
SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf

Este documento presenta una lección sobre las leyes de los gases ideales. Introduce los conceptos clave como condiciones normales, volumen molar y ecuaciones de estado. Explica las leyes de Boyle, Charles y Gay-Lussac y cómo se combinan en la ecuación general de los gases ideales. Finalmente, incluye ejercicios de aplicación de estas leyes a problemas numéricos sobre volumen, presión y temperatura de gases.
7 7 leyesdelosgasesideales

El documento describe las leyes de los gases ideales, incluyendo la ecuación de estado PV=nRT y las leyes de Boyle-Mariotte, Charles y Gay-Lussac. Explica que la presión y el volumen son inversamente proporcionales según la ley de Boyle, mientras que el volumen y la temperatura, y la presión y la temperatura, son directamente proporcionales según las leyes de Charles y Gay-Lussac, respectivamente. También incluye ejercicios de cálculo para aplicar estas leyes.
01 termoquímica

El documento describe conceptos fundamentales de termoquímica como sistemas, estados, funciones de estado, primer y segundo principios de la termodinámica, energía interna, entalpía, entalpía estándar de reacción y formación. También explica cómo calcular las variaciones de energía interna y entalpía en reacciones químicas y la aplicación de la ley de Hess.
ATOMO Y MATERIA.ppt

El documento trata sobre los conceptos básicos de materia, sus propiedades y los diferentes estados. Explica que la materia es todo aquello que tiene masa y ocupa un espacio, y que puede encontrarse en estado sólido, líquido o gaseoso. También describe las sustancias puras como elementos o compuestos químicos, y las mezclas como homogéneas u heterogéneas. Por último, introduce conceptos como átomo, molécula y algunas aleaciones comunes.
DIRECCION ELECTRICA.pptx

1) La dirección asistida eléctricamente reemplaza los componentes hidráulicos con un sensor de par, motor eléctrico y computador. 2) Reduce el consumo de combustible al accionar el motor eléctrico solo cuando se necesita. 3) Es más compleja de reparar que los sistemas hidráulicos tradicionales y se recomienda llevarlos a servicios técnicos autorizados.
Más contenido relacionado
Similar a PRESION EN LOS GASES.ppt
Tfb03 gases i

El documento describe las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Gay-Lussac. Explica que un gas ideal se compone de moléculas perfectamente elásticas que interactúan débilmente. Las leyes relacionan la presión, volumen y temperatura de un gas, y son importantes para entender las propiedades de los gases y su comportamiento.
Estado gaseoso

1) La ecuación NaN3(s) → Na(s) + N2(g) representa la descomposición del azida sódico en sodio sólido y nitrógeno gaseoso.
2) El documento fue compilado por Alexánder Gutiérrez M. y Roberto Gutiérrez P. como parte de su programa de licenciatura en biología y química.
3) Se proporciona información sobre los diferentes estados de la materia, propiedades de los gases, leyes de los gases y teoría cinética molecular.
Estado gaseoso

El documento describe la descomposición del azida de sodio en sodio metálico y nitrógeno gaseoso. Explica que el azida de sodio se descompone en sodio sólido y nitrógeno gaseoso. También incluye los nombres de los autores que compilaron la información.
ESTADOGASPPT

El documento describe las propiedades de los gases y la teoría cinética molecular. Según la teoría, los gases están compuestos de partículas en constante movimiento que se mueven libremente y chocan entre sí. Las propiedades de los gases, como su expansibilidad y compresibilidad, se deben a la gran distancia entre las moléculas. La teoría también explica cómo las variables de estado como la presión, el volumen y la temperatura están relacionadas a través de las leyes de los gases ideales.
presentacionleyesdelosgases-100114093741-phpapp02.pptx

Este documento presenta las leyes fundamentales de los gases y la teoría cinética molecular. Explica las leyes de Avogadro, Boyle y Mariotte, y Charles y Gay-Lussac, así como la ecuación general de los gases ideales. También describe el modelo molecular que explica estas leyes en términos del movimiento y las colisiones de las partículas que componen los gases. Finalmente, incluye un apéndice sobre recursos educativos relacionados con las leyes de los gases.
04 Gases 21 03 05

El documento resume las principales leyes de los gases, incluyendo la ley de Boyle, la ley de Charles, la ley de Avogadro y la ley de los gases ideales. Explica que la presión y el volumen de los gases están inversamente relacionados a temperatura constante según la ley de Boyle, y que el volumen de los gases es directamente proporcional a la temperatura a presión constante según la ley de Charles. También cubre conceptos como el volumen molar y la densidad de los gases.
Cap 1 gases

1) La termodinámica estudia las propiedades de los gases, las leyes de los gases ideales y reales, y el equilibrio químico.
2) La teoría cinético molecular explica el comportamiento de los gases usando un modelo en el que las moléculas se mueven rápidamente y se golpean entre sí y las paredes del contenedor.
3) Las ecuaciones de estado relacionan variables de estado como la presión, volumen y temperatura para describir el comportamiento de los gases. La ecuación del gas ideal es una aproximación pero
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...CristianQuispeCerron
El documento presenta las propiedades empíricas de los gases, incluyendo las leyes de Boyle, Charles, Gay-Lussac y Avogadro. Explica la ecuación de estado de los gases ideales y cómo se relacionan el volumen, la presión, la temperatura y la cantidad de sustancia. También cubre conceptos como la constante de los gases, la distribución barométrica y ejercicios prácticos sobre la aplicación de estas leyes.Diapositivas gases

El documento describe la composición de la atmósfera terrestre y los gases que contiene además del nitrógeno y oxígeno mayoritarios. Explica las propiedades de los gases y las leyes que rigen su comportamiento, incluyendo las leyes de Boyle, Charles y Gay-Lussac, así como la teoría cinética de los gases y el concepto de gases ideales.
Leyes gases 1

Este documento resume las leyes fundamentales de los gases ideales y reales. Explica que un gas se define por su volumen, presión, temperatura y cantidad de sustancia. A continuación, describe las leyes de Avogadro, Boyle, Charles y Gay-Lussac, y la ecuación general de los gases ideales PV=nRT. También cubre el comportamiento real de los gases mediante la ecuación de Van der Waals y la ley de Dalton de las presiones parciales.
Fiqui estado gaseoso

El documento describe los conceptos fundamentales del estado gaseoso y el modelo del gas ideal. Explica las leyes de Boyle, Charles y Gay-Lussac, y la ecuación de estado del gas ideal. También cubre temas como mezclas de gases, humedad en el aire, y desviaciones del comportamiento ideal observadas en gases reales.
Física (II Bimestre)

Universidad Técnica Particular de Loja
Gestión Ambiental
Física
II Bimestre
Abril-Agosto 2007
Ponente: Mg. Henry Quezada
Leyes De Los Gases

El documento describe las leyes de los gases, incluyendo la Ley de Boyle, la Ley de Charles y la Ley de Gay-Lussac. Explica que la presión y el volumen de un gas varían inversamente a temperatura constante según la Ley de Boyle, y varían directamente con la temperatura a presión o volumen constante según las Leyes de Charles y Gay-Lussac, respectivamente.
Tema 2

1) El documento describe las leyes de los gases ideales, incluyendo las leyes de Boyle, Charles y Gay-Lussac, y la ley combinada de los gases. 2) Explica cómo estas leyes se pueden usar para derivar la ecuación de estado de los gases ideales. 3) También cubre conceptos como presión parcial, volumen molar y densidad de los gases.
Laboratorio de gases ideales

Este documento presenta información sobre los gases ideales, incluyendo sus estados, leyes y fórmulas. Explica las leyes de Boyle, Charles, Gay-Lussac y la ley generalizada de los gases, además de realizar ejercicios prácticos aplicando estas leyes. El objetivo es ayudar a los estudiantes a comprender mejor los conceptos fundamentales relacionados con los gases ideales.
Teoria de los gases ideales comportamiento

Este documento describe las propiedades de los gases ideales y reales. Los gases ideales se comportan de manera ideal a presiones bajas y altas temperaturas, mientras que los gases reales se comportan de manera no ideal a presiones altas y bajas temperaturas. También explica las leyes de Boyle, Charles y Avogadro, y presenta la ecuación de estado de los gases ideales.
Las leyes de los gases.

El documento resume las principales leyes de los gases. La ley de Boyle establece que a temperatura constante, el volumen de un gas es inversamente proporcional a la presión. La ley de Charles establece que a presión constante, el volumen de un gas es directamente proporcional a la temperatura absoluta. La ley de Gay-Lussac establece que a volumen constante, la presión de un gas es directamente proporcional a la temperatura absoluta. Las tres leyes se combinan en la ecuación general de los gases ideales, donde la presión
SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf

Este documento presenta una lección sobre las leyes de los gases ideales. Introduce los conceptos clave como condiciones normales, volumen molar y ecuaciones de estado. Explica las leyes de Boyle, Charles y Gay-Lussac y cómo se combinan en la ecuación general de los gases ideales. Finalmente, incluye ejercicios de aplicación de estas leyes a problemas numéricos sobre volumen, presión y temperatura de gases.
7 7 leyesdelosgasesideales

El documento describe las leyes de los gases ideales, incluyendo la ecuación de estado PV=nRT y las leyes de Boyle-Mariotte, Charles y Gay-Lussac. Explica que la presión y el volumen son inversamente proporcionales según la ley de Boyle, mientras que el volumen y la temperatura, y la presión y la temperatura, son directamente proporcionales según las leyes de Charles y Gay-Lussac, respectivamente. También incluye ejercicios de cálculo para aplicar estas leyes.
01 termoquímica

El documento describe conceptos fundamentales de termoquímica como sistemas, estados, funciones de estado, primer y segundo principios de la termodinámica, energía interna, entalpía, entalpía estándar de reacción y formación. También explica cómo calcular las variaciones de energía interna y entalpía en reacciones químicas y la aplicación de la ley de Hess.
Similar a PRESION EN LOS GASES.ppt (20)
presentacionleyesdelosgases-100114093741-phpapp02.pptx

presentacionleyesdelosgases-100114093741-phpapp02.pptx
S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...

S2 EYES - BOYLE - LUSSAC- ECUACION DE ESTADO - DISRTRIBUCION BAROMETRICA - EJ...
SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf

SEMANA N° 10 Quimica General - Mg. MIGUEL VASQUEZ HUAMAN.pdf
Más de sarengo
ATOMO Y MATERIA.ppt

El documento trata sobre los conceptos básicos de materia, sus propiedades y los diferentes estados. Explica que la materia es todo aquello que tiene masa y ocupa un espacio, y que puede encontrarse en estado sólido, líquido o gaseoso. También describe las sustancias puras como elementos o compuestos químicos, y las mezclas como homogéneas u heterogéneas. Por último, introduce conceptos como átomo, molécula y algunas aleaciones comunes.
DIRECCION ELECTRICA.pptx

1) La dirección asistida eléctricamente reemplaza los componentes hidráulicos con un sensor de par, motor eléctrico y computador. 2) Reduce el consumo de combustible al accionar el motor eléctrico solo cuando se necesita. 3) Es más compleja de reparar que los sistemas hidráulicos tradicionales y se recomienda llevarlos a servicios técnicos autorizados.
ALINEAMIENTO DE DIRECCION ALL.ppt

El documento describe los diferentes aspectos de la alineación de las ruedas de un vehículo, incluyendo el ángulo de caída, el avance del pivote, la inclinación del eje de dirección y la base. Explica que estos cinco factores deben estar alineados correctamente para garantizar un rendimiento estable y seguro del vehículo en línea recta y en curvas. Una mala alineación puede causar problemas como una dirección difícil o poco estable.
ENEMIGOS DEL CARRO.pptx

El documento describe los enemigos y amigos de los autos. Los enemigos, como el alquitrán, lluvias ácidas, polvo y rayos UV, dañan los autos a largo plazo. Los amigos, como el shampoo, cera y silicona, ayudan a cuidar y proteger los autos cuando se les da mantenimiento regular. El documento también explica cómo el pH afecta la capacidad de diferentes productos para limpiar sin dañar la pintura de los autos.
CERAS.ppt

Este documento describe diferentes tipos de ceras y productos de silicona utilizados para el cuidado de autos. Incluye ceras para acabado de pintura, limpieza de interiores y exteriores, así como siliconas líquidas y en aerosol para limpiar y proteger tableros, asientos y neumáticos. También proporciona instrucciones para la aplicación correcta de estos productos químicos.
aceites y grasas direccion.ppt

El documento describe los diferentes tipos de aceites y grasas lubricantes, incluyendo su composición, clasificación y propiedades. Los aceites lubricantes se componen de una base como derivados del petróleo o químicos, así como aditivos que mejoran sus propiedades. Las grasas se componen de una solución jabonosa en aceite mineral y varían según el compuesto de jabón utilizado, como jabón de calcio, sodio o bentonita. Tanto los aceites como las grasas cumplen funciones como lubricar, disipar calor y ev
2 Sistemas Dirección Suspensión 1.ppt

Este documento presenta información sobre sistemas de dirección y suspensión. Explica los componentes clave de la dirección como el volante, columna de dirección y varillaje. También describe los tipos de mecanismos de dirección como salida rotativa y piñón y cremallera. Finalmente, introduce conceptos básicos sobre suspensión como resortes, amortiguadores y movimientos de la carrocería.
Más de sarengo (7)
Último
sistema de encendido transistorizado sin contacto por induccion.pdf

sistema de encendido transistorizado sin contacto por inducción
COMPLETO trabajo para realizarun proyecto de grato de mecanica automotriz(1)...

una manera de realizar un proyecto de mecanica automotriz para un mejor rendimiento y una pista de como se deve realizar un proyecto
Último (8)
sistema de encendido transistorizado sin contacto por induccion.pdf

sistema de encendido transistorizado sin contacto por induccion.pdf
COMPLETO trabajo para realizarun proyecto de grato de mecanica automotriz(1)...

COMPLETO trabajo para realizarun proyecto de grato de mecanica automotriz(1)...
PRESION EN LOS GASES.ppt
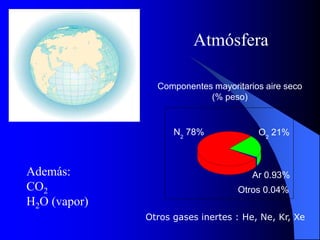
- 1. Otros 0.04% Ar 0.93% O2 21% N2 78% Componentes mayoritarios aire seco (% peso) Otros gases inertes : He, Ne, Kr, Xe Atmósfera Además: CO2 H2O (vapor)
- 2. 11 elementos He, Ne, Ar, Kr, Xe, Rn, H2, N2, O2, O3, F2, Cl2 Compuestos moleculares: CO, CO2, HCl, NH3, CH4, NO, NO2, N2O,SO2, SO3, HCN. GAS Estado gaseoso a temperaturas y presiones ordinarias. VAPOR forma gaseosa de cualquier sustancia que es líquida ó sólida a temperaturas y presiones ordinarias.
- 3. Ecuación de estado: V = V (T, P, n) Volumen (sólido, líquido, gas) depende de Temperatura (T) Presión (P) Liquídos y sólidos Ecuación de estado muy complicadas y difieren considerablemente de una sustancia a otra.
- 4. • se pueden comprimir • ocupan todo el espacio disponible MOLÉCULAS • Separadas • Movimiento caótico Gases Ecuación de estado universal. • moléculas casi independientes unas de otras • la naturaleza particular no afecta el comportamiento general
- 5. Presión de un gas Un gas ejerce presión sobre una superficie debido al choque de las moléculas sobre ella.
- 7. Barómetro Atmósfera estándar: Presión ejercida por una columna de Hg de 76 cm de longitud y de densidad 13,5951 g/cm3 en un lugar en donde g es 980,665 cm/s2
- 8. Unidades F P A 1 Pa = 1 N/m2 P h g 1 atm = 760 mmHg = 760 torr 1 atm = 101325 Pa = 1.013 x 105 Pa = 1.013 x 102 kPa
- 9. Ejercicio Calcular la equivalencia entre una atmósfera estándar y Pa. Recordar que una atm es la presión ejercida por una columna de Hg de 76 cm de longitud y de densidad 13,5951 g/cm3 en un lugar en donde g es 980,665 cm/s2 F P A
- 10. Presión de un gas Caso A Pgas = Pext Caso B Pgas = Pext + h Caso C Pgas = Pext - h
- 11. LEYES DE LOS GASES Ecuación de estado: V = V (T, P, n) LEY DE CHARLES (V constante) LEY DE BOYLE-MARIOTTE (T constante) LEY DE AVOGADRO (T y P constantes) LEY DE GAY-LUSSAC (P constante)
- 12. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE
- 13. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE
- 14. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE p V = constante p = constante / V p1V1 = p2V2
- 15. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE p = constante / V
- 16. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE p = constante / V
- 17. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE p = constante / V ISOTERMAS
- 18. LEY DE BOYLE-MARIOTTE TEMPERATURA CONSTANTE Ejercicios 1.- Una masa dada de gas ocupa un volumen de 240 ml a 1.25 atm, ¿cuál será el cambio de volumen si la presión se llevara a 0.75 atm a la misma T? 2.- Un globo inflado tiene un volumen de 0.55 l al nivel del mar (1 atm) y se deja elevar a una altura de 6.5 km, donde la presión es de unos 0.40 atm. Considerando que la temperatura permanece constante, ¿cuál es el volumen final del globo?
- 19. LEY DE CHARLES PRESIÓN CONSTANTE P atm Termómetro 0 OC Vo aire P atm Termómetro 100 OC V100 Vt
- 20. LEY DE CHARLES PRESIÓN CONSTANTE Vt = Vo + (v × Vo) t = Vo (1 + v × t) Coeficiente de dilatación a presión constante a bajas presiones y altas temperaturas, a v = 1/273 °C-1
- 21. LEY DE CHARLES PRESIÓN CONSTANTE V = constante × T
- 22. LEY DE CHARLES PRESIÓN CONSTANTE V = constante × T ISOBARAS
- 23. LEY DE CHARLES PRESIÓN CONSTANTE
- 24. LEY DE CHARLES PRESIÓN CONSTANTE Escala absoluta de temperatura: T (K), el 0 K es la temperatura más baja posible ya que el gas tendría V = 0 a esa temperatura, y cualquier temperatura menor a 0 K correspondería a V < 0.
- 25. LEY DE CHARLES PRESIÓN CONSTANTE
- 26. LEY DE GAY-LUSSAC VOLUMEN CONSTANTE P = constante × T
- 27. LEY DE GAY-LUSSAC VOLUMEN CONSTANTE ISOCORAS
- 28. Ejercicios Expresar la ley de Charles y la de Gay-Lussac en la escala absoluta de temperaturas. Encontrar la relación entre V y P. Vt = Vo + (v × Vo) t = Vo (1 + v × t) Ley de Charles Pt = Po + (P × Po) t = Po (1 + P × t) Ley de Gay-Lussac
- 29. LEY DE AVOGADRO PRESIÓN Y TEMPERATURA CONSTANTES VOLÚMENES MOLARES a 0OC y 1 atm EL VOLUMEN DE GAS ES DIRECTAMENTE PROPORCIONAL AL NÚMERO DE MOLÉCULAS
- 30. LEY DE CHARLES (P constante) V / T = cte2 LEY DE BOYLE-MARIOTTE (T constante) P V = cte1 LEY DE AVOGADRO (T y P constantes) V / n = cte4 LEY DE GAY-LUSSAC (V constante) P / T = cte3 GAS IDEAL CUMPLE CON LAS LEYES DE LOS GASES EN TODO INTERVALO DE PRESIÓN Y TEMPERATURA
- 31. Ley del gas ideal Ecuación de estado del gas ideal P V = n R T Constante de los gases P constante V / T = cte2 T constante P V = cte1 T y P constantes V / n = cte4 V constante P / T = cte3
- 32. Ley del gas ideal Ecuación de estado del gas ideal P V = n R T Constante de los gases Valores de R 8.314 107 erg / K mol 8.314 J / K mol 1.987 cal / K mol 0,082 l atm / K mol
- 33. CPTA: Condiciones de Presión y Temperatura Ambiente 25.00 °C y 1 bar CNTP: Condiciones Normales de Temperatura y Presión 0 °C y 1 atm
- 34. Ejercicio Calcular la presión dentro de un tubo de televisión sabiendo que el volumen es 5.0 l, su temperatura 23°C y que contiene 0.010 mg de N2.