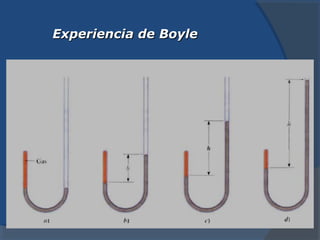
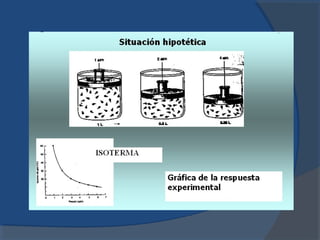
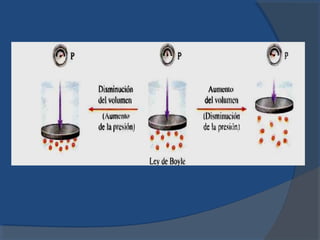
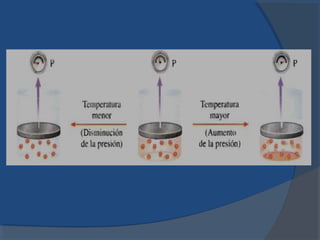
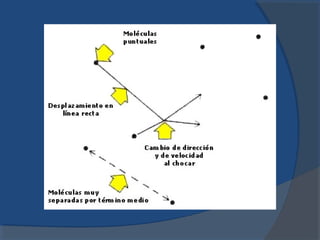
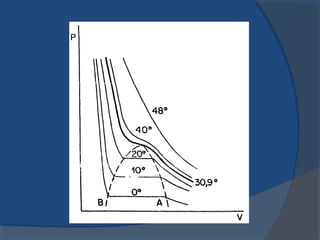
El documento describe la composición de la atmósfera terrestre y los gases que contiene además del nitrógeno y oxígeno mayoritarios. Explica las propiedades de los gases y las leyes que rigen su comportamiento, incluyendo las leyes de Boyle, Charles y Gay-Lussac, así como la teoría cinética de los gases y el concepto de gases ideales.