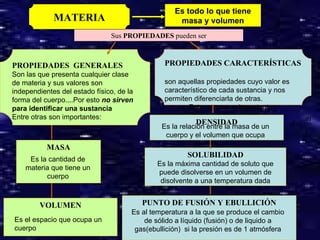
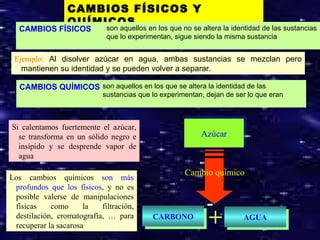
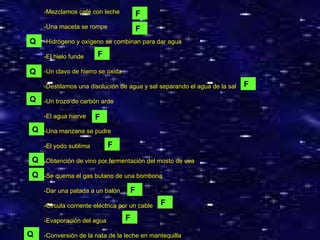
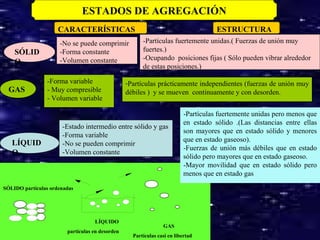
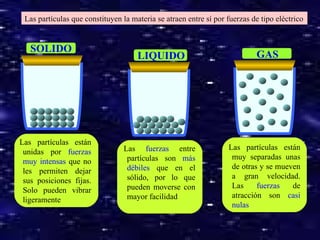
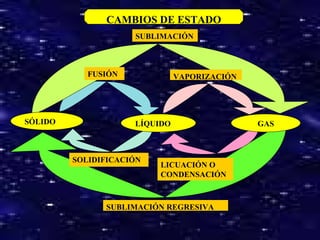
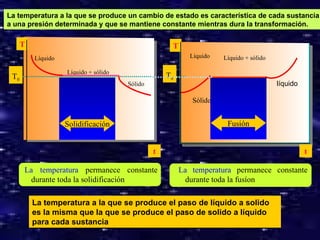
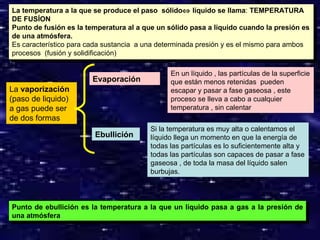
El documento describe las propiedades generales y características de la materia. Las propiedades generales incluyen masa, volumen y densidad, mientras que las propiedades características permiten diferenciar sustancias como punto de fusión, solubilidad y punto de ebullición. La materia puede existir en tres estados de agregación - sólido, líquido y gas - dependiendo de la estructura molecular, fuerzas intermoleculares y movimiento de las partículas. Los cambios de estado incluyen fusión, solidificación, vaporización y condens