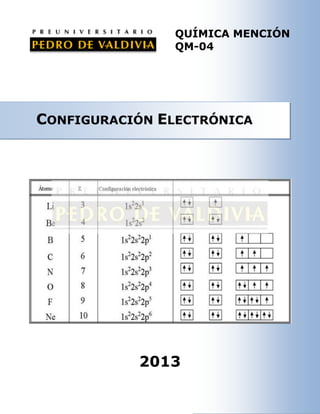
El documento describe la configuración electrónica de los electrones en átomos, utilizando números cuánticos para identificar sus estados energéticos. Se detalla el principio de construcción de Aufbau, la exclusión de Pauli, y la regla de máxima multiplicidad de Hund para la distribución de electrones. Además, se incluye un resumen de la configuración electrónica de los 30 primeros elementos del sistema periódico.