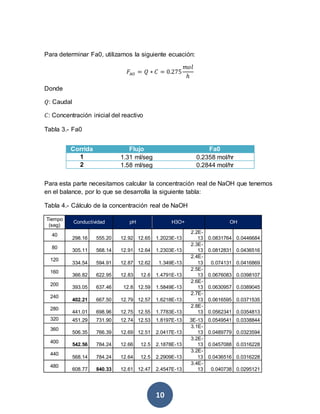
Este documento describe un experimento para simular un reactor CSTR utilizando dos sistemas diferentes. Se prepararon soluciones de acetato de etilo y hidróxido de sodio y se midió la conductividad a intervalos de tiempo. Los resultados se utilizaron para calcular la concentración real de NaOH y la constante de velocidad de la reacción de segundo orden. El análisis indica que ambos sistemas funcionaron para simular un reactor CSTR y la reacción siguió una cinética de segundo orden.











![14
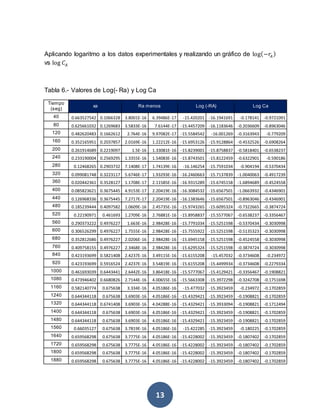
Ahora, procedemos a graficar los datos, se presentan a continuación:
Por lo tanto la ecuación cinética es
−𝑟𝐴 = 10−3.2295
𝐶𝐴
1
[
𝑚𝑜𝑙
𝐿 ℎ
]
−𝑟𝐴 = 5.86 ∗ 10−4
𝐶𝐴
1
[
𝑚𝑜𝑙
𝐿 𝑚𝑖𝑛
]
La ecuación reportada por la literatura a 30°C es
−𝑟𝐴 = 4.54 𝐶𝐴
2
[
𝑚𝑜𝑙
𝐿 𝑚𝑖𝑛
]
y = x - 3.2295
R² = 1
-6
-5
-4
-3
-2
-1
0
-1.8 -1.6 -1.4 -1.2 -1 -0.8 -0.6 -0.4 -0.2 0
Log-Ra
LOG Ca
Grafico 5.- Log Ca vs Log -Ra (1)](https://image.slidesharecdn.com/reporte-reactor-cstr-170621170308/85/Reporte-reactor-cstr-14-320.jpg)
![15
Por lo tanto la ecuación cinética es
−𝑟𝐴 = 10−3.1481
𝐶𝐴
1
[
𝑚𝑜𝑙
𝐿 ℎ
]
−𝑟𝐴 = 7.11049 ∗ 10−4
𝐶𝐴
1.9107
[
𝑚𝑜𝑙
𝐿 𝑚𝑖𝑛
]
y = 1x - 3.1481
R² = 1
-4.5
-4
-3.5
-3
-2.5
-2
-1.5
-1
-0.5
0
-1.2 -1 -0.8 -0.6 -0.4 -0.2 0
Log-Ra
LOG Ca
Grafico 6.- Log Ca vs Log -Ra (2)](https://image.slidesharecdn.com/reporte-reactor-cstr-170621170308/85/Reporte-reactor-cstr-15-320.jpg)

