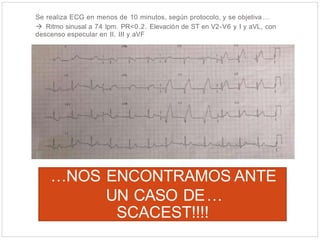
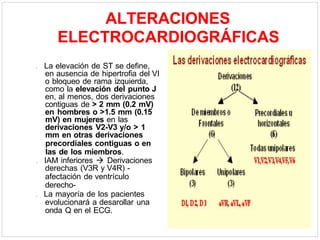
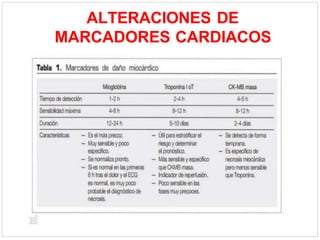
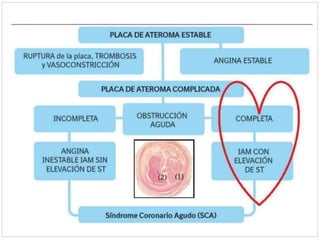
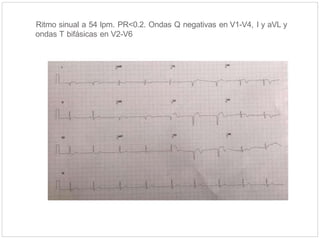
Este documento describe el caso de un hombre de 29 años que acude a urgencias con dolor torácico opresivo de 90 minutos de evolución. Tras realizar un electrocardiograma se diagnostica un síndrome coronario agudo con elevación del segmento ST (SCACEST). El documento resume la definición, diagnóstico, factores de riesgo, alteraciones electrocardiográficas, marcadores cardiacos y tratamiento del SCACEST, incluyendo opciones de reperfusión como la fibrinólisis o la angioplastia coronaria primaria. Final