Incrustar presentación
Descargado 85 veces




















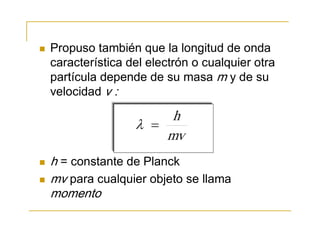
















































































El documento presenta información sobre varios temas relacionados con la física cuántica, incluyendo el efecto fotoeléctrico, la dualidad onda-partícula de la luz, la teoría cuántica de Planck, el modelo atómico de Bohr, la naturaleza ondulatoria de la materia según de Broglie, el principio de incertidumbre de Heisenberg y los números cuánticos.



































































































