Este documento trata sobre el equilibrio químico. Explica que las reacciones reversibles alcanzan un estado de equilibrio dinámico donde la velocidad de formación de productos es igual a la de formación de reactivos. También define la constante de equilibrio K como una relación entre las concentraciones de sustancias en el equilibrio que permanece constante si no cambia la temperatura. Por último, explica cómo evoluciona un sistema químico hacia el equilibrio dependiendo de si el cociente de reacción Q es menor, igual o mayor que K



![3. CONSTANTE DE EQUILIBRIO
El sistema 2 NO2
N2
O4
a 25 ºC:
CONCENTRACIONES
INICIALES (M)
CONCENTRACIONES EN
EL EQUILIBRIO (M)
RELACIÓN DE
CONCENTRACIONES EN
EL EQUILIBRIO
[NO2
] [N2
O4
] [NO2
] [N2
O4
]
[NO2
]
[N2
O4
]
[NO2
]2
[N2
O4
]
0,000 0,670 0,0547 0,643 0,0851 4,65·10-3
0,0500 0,446 0,0457 0,448 0,102 4,66·10-3
0,0300 0,500 0,0475 0,491 0,0967 4,60·10-3
0,0400 0,600 0,0523 0,594 0,0880 4,60·10-3
0,200 0,000 0,0204 0,0898 0,227 4,63·10-3](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-4-320.jpg)
![3. CONSTANTE DE EQUILIBRIO
El sistema 2 NO2
N2
O4
a 25 ºC:
CONCENTRACIONES
INICIALES (M)
CONCENTRACIONES EN
EL EQUILIBRIO (M)
RELACIÓN DE
CONCENTRACIONES EN
EL EQUILIBRIO
[NO2
] [N2
O4
] [NO2
] [N2
O4
]
[NO2
]
[N2
O4
]
[NO2
]2
[N2
O4
]
0,000 0,670 0,0547 0,643 0,0851 4,65·10-3
0,0500 0,446 0,0457 0,448 0,102 4,66·10-3
0,0300 0,500 0,0475 0,491 0,0967 4,60·10-3
0,0400 0,600 0,0523 0,594 0,0880 4,60·10-3
0,200 0,000 0,0204 0,0898 0,227 4,63·10-3
PRÁCTICAMENTE
CONSTANTE](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-5-320.jpg)
![3. CONSTANTE DE EQUILIBRIO
El sistema 2 NO2
N2
O4
a 25 ºC:
K es una constante para la reacción en equilibrio:
N2
O4
(g) 2 NO2
(g) a 25 ºC
El exponente 2 de [NO2
] y el exponente 1 del [N2
O4
] coinciden con
los coeficientes de la ecuación química.
K = = 4,63·10-3
[NO2
]2
[N2
O4
]](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-6-320.jpg)
![LEY DE ACCIÓN DE MASAS
Para una reacción reversible a una temperatura dada:
Siendo a, b, c y d los coeficientes estequiométricos de las sustancias A, B, C y
D.
K es la constante de equilibrio y [A], [B], [C] y [D] son las concentraciones de
estas sustancias en el equilibrio.
K no tiene unidades.
aA + bB cC + dD
K =
[C]c
· [D]d
[A]a
· [B]b](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-7-320.jpg)

![EJEMPLO
CO (g) + 2 H2
(g) CH3
OH (g)
Condiciones
T = 483 K
V = 10 L
CONCENTRACIONES
INICIALES (M)
CONCENTRACIONES EN
EL EQUILIBRIO (M)
[CO] [H2
] [CH3
OH] [CO]eq
[H2
]eq
[CH3
OH]eq
EXP. 1 0,1 0,1 0 0,0911 0,0822 0,0892 14,5
EXP. 2 0 0 0,1 0,0753 0,151 0,0247 14,5
EXP. 3 0,1 0,1 0,1 0,138 0,176 0,0620 14,5
[CH3
OH]
[H2
]2
· [CO]](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-9-320.jpg)
![EJEMPLO
CO (g) + 2 H2
(g) CH3
OH (g)
A temperatura constante, el valor de K es independiente de la forma en que se
alcanzó el equilibrio.
La composición del sistema en el equilibrio depende de la composición de
partida y cumple la condición:
KC
= = 14,5
[CH3
OH]
[H2
]2
· [CO]](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-10-320.jpg)


![FORMAS DE EXPRESAR LA CONSTANTE DE EQUILIBRIO
Para emplear constantes de equilibrio es necesario expresarlas en términos
de concentraciones de reactivos y productos.
Las concentraciones se pueden expresar en distintas unidades, por lo que hay
más de un modo de expresar la constante de equilibrio de la misma reacción.
aA + bB cC + dD
El subíndice de KC
indica que las concentraciones en el equilibrio de las
sustancias que intervienen en la reacción se expresar en molaridad (mol/L).
Sólo se incluyen las especies gaseosas y/o en disolución.
Las especies en estado sólido o líquido tienen concentración constante y no
se incluyen en la constante de equilibrio.
KC
=
[C]c
· [D]d
[A]a
· [B]b
KC](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-13-320.jpg)

![RELACIÓN ENTRE KC
Y KP
p · V = n · R · T c = =
En el equilibrio:
n
V
p
R · T
KC
= = = · (R · T)[-(c + d) + (a + b)]
= · (R · T)-Dn
[C]c
· [D]d
[A]a
· [B]b
pC
R · T
pD
R · T
·
·
C D
pA
R · T
A
pB
R · T
B
pc
c
·pD
d
pA
a
·pB
b
pc
c
·pD
d
pA
a
·pB
b
KP
= KC
· (R · T)Dn
KC
= KP
· (R · T)-Dn
En general, KC
≠ KP
, excepto en el caso especial en el que Dn = 0.](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-15-320.jpg)

![4. EVOLUCIÓN HACIA EL EQUILIBRIO
COCIENTE DE REACCIÓN
Para una reacción química:
aA + bB cC + dD
● La expresión de Q coincide con la de K.
● El valor de Q es diferente al de K.
● El valor de Q es variable en el tiempo mientras que el de K permanece
constante.
Q =
[C]c
· [D]d
[A]a
· [B]b
no equilibrio
El sistema evolucionará para
alcanzar el equilibrio, de modo que
Q adquiera el valor de K.
El valor de Q permite predecir en
qué sentido evolucionará la
reacción para alcanzar el
equilibrio.](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-17-320.jpg)

![EJEMPLO
COCl2
(g) CO (g) + Cl2
(g), KC
(100 ºC) = 2,2·10-10
MEZCLA A B C
[CO]0 1,0·10-3
M 3,31·10-6
M 4,50·10-7
M
[Cl2
]0 1,0·10-3
M 3,31·10-6
M 5,73·10-6
M
[COCl2
]0 2,19·10-1
M 5,00·10-2
M 8,57·10-2
M
Q =
[CO] · [Cl2
]
[COCl2
]
QA
= 4,6·10-6
QB
= 2,2·10-10
QC
= 3,0·10-11
QA
> K QB
= K QC
< K
R P En equilibrio R P](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-19-320.jpg)


![EJEMPLO 1
N2
O4
(g) 2 NO2
(g) , KC
=
[NO2
]2
[N2
O4
]
Las concentraciones en el equilibrio de N2
O4
y NO2
:
Calculamos KC
sustituyendo en su expresión los valores de las concentraciones
de las sustancias en el equilibrio:
[NO2
]2
[N2
O4
]
KC
= = = 4,61·10-3
(0,0113)2
0,0277
[N2
O4
] = = 0,0277 M
[NO2
] = = 0,013 M
7,64 g ·
1 mol N2
O4
1 mol NO2
1,56 g ·
46,01 g
12,01 g
3 L
3 L](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-22-320.jpg)

![EJEMPLO 2
N2
(g) + 3 H2
(g) 2 NH3
(g)
t = 0: 4 12 -
teq
: 4 – x 12 – 3x 2x
x = 0,46 mol: 3,54 10,62 0,92 mol
[ ]eq
(M): 0,354 1,062 0,092
[NH3
]2
[N2
] · [H2
]3
KC
= = = 1,996·10-2
0,0922
0,354 · (1,062)2](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-24-320.jpg)
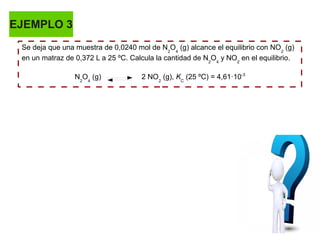
![EJEMPLO 3
N2
O4
(g) 2 NO2
(g)
t = 0: 0,0240 -
teq
: 0,024 – x 2x
[ ]eq
(M): 0,024 - x 2x
[NO2
]2
[N2
O4
]
KC
= = x = 3,00·10-3
0,372 0,372
0,372
0,372
2x
2
0,024 - x
n (N2
O4
)eq
= 0,0240 – 3,00·10-3
= 0,0210 mol
n (NO2
)eq
= 2 · 3,00·10-3
= 6,00·10-3
mol](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-26-320.jpg)


![EJEMPLO 4
PCl5
(g) PCl3
(g) + Cl2
(g)
t = 0: 2 1 -
teq
: 2 – x 1 + x x
[ ]eq
(M): 2 - x 1+ x x
[PCl3
]·[Cl2
]
[PCl5
]
KC
= = = 0,042 x = 0,28 moles
5 5
5
5
1+ x
2 - x
5
5
x
[PCl5
] = 0,342 M; [PCl3
] = 0,256 M; [Cl2
] = 0,056 M
a = = 0,14
0,28 mol
2 mol](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-29-320.jpg)




![EJEMPLO 6
4 CuO (s) 2 Cu2
O (s) + O2
(g)
t = 0: 2 mol - -
teq
: 2 – 4x 2x x
KP
= P (O2
) = 0,49 atm
P (O2
) = = [O2
]·R·T [O2
] = = = 0,0046 M
n(Cu2
O) = 2 - 4·x = 1,96 mol
x = 0,046 mol · 2 L = 0,092 mol
m(CuO)eq
= 1,969 mol · 79,5 g = 156,1 g
n(O2
)·R·T
V
P(O2
)
R·T
0,49
0,082·1297
L
1 mol](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-34-320.jpg)
![EJEMPLO 7
El NH4
HS (s) utilizado en el revelado de fotografías, es inestable y se descompone a
temperatura ambiente:
NH4
HS (s) NH3
(g) + H2
S (g), KP
(25 ºC) = 0,108
Se introduce una muestra en un recipiente a 25 ºC, en el que se ha hecho el vacío.
¿Cuál es la presión total del gas en el equilibrio?
KP
= P(NH3
) · P(H2
S) = P(NH3
) · P(NH3
) = [P(NH3
)]2
= 0,108 P(NH3
) = P(H2
S) = 0,329 atm
P(NH3
) = P(H2
S)
PT
= P(NH3
) + P(H2
S) = 0,658 atm](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-35-320.jpg)

![CAMBIO EN LA CONCENTRACIÓN DE REACTIVOS Y/O PRODUCTOS
El sistema tiende a alcanzar un nuevo estado de equilibrio:
● Si a un sistema en equilibrio SE LE AGREGA un reactivo o producto en
exceso, el sistema evoluciona de manera de CONSUMIR dicho exceso.
● Si a un sistema en equilibrio SE LE EXTRAE un reactivo o producto, el
sistema evoluciona de manera de PRODUCIR esa especie y compensar
ese defecto.
Se perturba el equilibrio cuando:
a) Se adiciona producto: El equilibrio se desplaza hacia la izquierda, para
consumir parte del reactivo (Q > K).
b) Se adiciona reactivo: El equilibrio se desplaza hacia la derecha, para
consumir parte del producto (Q < K).
KC
=
[C]c
· [D]d
[A]a
· [B]b
aA (g) + bB (g) cC (g) + dD (g),](https://image.slidesharecdn.com/tema6-170625144943/85/Tema-6-Equilibrio-quimico-37-320.jpg)




