Problema reacción química obtención urea
•Descargar como PPTX, PDF•
2 recomendaciones•14,392 vistas
Problema resuelto de obtención de urea a partir del amoniaco. Se determina el rendimiento de la reacción y el tanto por ciento de nitrógeno en la urea.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...

45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...María Victoria Arques Galiana
Más contenido relacionado
La actualidad más candente
45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...

45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...María Victoria Arques Galiana
La actualidad más candente (20)
45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...

45916215 quimica-ejercicios-resueltos-soluciones-2º-bachillerato-equilibrio-q...
Informe practica #3 (articulo cientifico), Clasificacion de sustancias organi...

Informe practica #3 (articulo cientifico), Clasificacion de sustancias organi...
Determinación de fórmulas químicas (empírica y molecular)

Determinación de fórmulas químicas (empírica y molecular)
Destacado
Destacado (6)
Reacción química de una caliza con ácido clorhídrico

Reacción química de una caliza con ácido clorhídrico
Similar a Problema reacción química obtención urea
Similar a Problema reacción química obtención urea (20)
Problema de reacción química obtención de acetileno

Problema de reacción química obtención de acetileno
Problema de reacción química obtención de acetileno

Problema de reacción química obtención de acetileno
Problema de reacción química obtención de acetileno

Problema de reacción química obtención de acetileno
4º - Estequiometría II - Problemas Serie 2 -qblog-2007

4º - Estequiometría II - Problemas Serie 2 -qblog-2007
Problema de reacción de disolución de h cl con mármol

Problema de reacción de disolución de h cl con mármol
Problema resuelto de análisis de un mármol y calcinación

Problema resuelto de análisis de un mármol y calcinación
Más de Diego Martín Núñez
Más de Diego Martín Núñez (20)
Problema resuelto reactivo limitante nitrato aluminio y sulfuro de h

Problema resuelto reactivo limitante nitrato aluminio y sulfuro de h
Problema resuelto reacción química riqueza y concentración

Problema resuelto reacción química riqueza y concentración
Problema de propiedad coligativa temperatura congelación de una disolución

Problema de propiedad coligativa temperatura congelación de una disolución
Problema de propiedad coligativa presión de vapor de una disolución

Problema de propiedad coligativa presión de vapor de una disolución
Problema de p h de una disolución de ácido benzoico y neutralización con hidr...

Problema de p h de una disolución de ácido benzoico y neutralización con hidr...
Problema de disolución reguladora amoniaco amónico

Problema de disolución reguladora amoniaco amónico
Problema de disolución reguladora acético acetato sin voz

Problema de disolución reguladora acético acetato sin voz
Problema de propiedad coligativa presión de vapor de una disolución

Problema de propiedad coligativa presión de vapor de una disolución
Pregunta curiosa qué ocurriría si una fuerza irresistible actuase sobre cuer...

Pregunta curiosa qué ocurriría si una fuerza irresistible actuase sobre cuer...
Cuando el hielo se derrite aumenta el nivel del agua o no sin voz

Cuando el hielo se derrite aumenta el nivel del agua o no sin voz
Último
Último (20)
Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...

Plan Refuerzo Escolar 2024 para estudiantes con necesidades de Aprendizaje en...
el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz

el CTE 6 DOCENTES 2 2023-2024abcdefghijoklmnñopqrstuvwxyz
la unidad de s sesion edussssssssssssssscacio fisca

la unidad de s sesion edussssssssssssssscacio fisca
SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf

SELECCIÓN DE LA MUESTRA Y MUESTREO EN INVESTIGACIÓN CUALITATIVA.pdf
DE LAS OLIMPIADAS GRIEGAS A LAS DEL MUNDO MODERNO.ppt

DE LAS OLIMPIADAS GRIEGAS A LAS DEL MUNDO MODERNO.ppt
La empresa sostenible: Principales Características, Barreras para su Avance y...

La empresa sostenible: Principales Características, Barreras para su Avance y...
Sesión de aprendizaje Planifica Textos argumentativo.docx

Sesión de aprendizaje Planifica Textos argumentativo.docx
Problema reacción química obtención urea
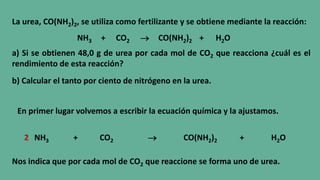
- 1. La urea, CO(NH2)2, se utiliza como fertilizante y se obtiene mediante la reacción: NH3 + CO2 CO(NH2)2 + H2O a) Si se obtienen 48,0 g de urea por cada mol de CO2 que reacciona ¿cuál es el rendimiento de esta reacción? b) Calcular el tanto por ciento de nitrógeno en la urea. En primer lugar volvemos a escribir la ecuación química y la ajustamos. NH3 + CO2 CO(NH2)2 + H2O2 Nos indica que por cada mol de CO2 que reaccione se forma uno de urea.
- 2. Hallamos el peso molecular de la urea. Pm(CO(NH2)2) = 12 + 16 + 14 · 2 + 1 · 4 = 60 g/mol La masa teórica de urea que debería obtenerse es de 60 g, pero como realmente se obtienen 48 g, el rendimiento ha sido: Rendimiento = m(CO(NH2)2) real · 100 m(CO(NH2)2) teórica = 48 g · 100 60 g = 80 %
- 3. CO(NH2)2 Pm(CO(NH2)2) = 12 + 16 + 14 · 2 + 1 · 4 = 60 g/mol De los 60 g de un mol de urea, 28, (2·14), son del nitrógeno. Por ello podemos calcular el tanto por ciento de nitrógeno en la urea. % N = m(N) · 100 m(CO(NH2)2) = 28 g · 100 60 g = 46,7 %
