Cómo obtener el nº de partículas subatómicas. ok
•Descargar como PPT, PDF•
3 recomendaciones•31,532 vistas
Power point que muestra gráficamente, mediante diapositivas animadas, la forma mediante la cual se cuenta el Nº de las partículas subatómicas de un átomo neutro o de un ión. Usando una hoja de trabajo dada por el profesor, el alumno debería practicar.
Denunciar
Compartir
Denunciar
Compartir
Recomendados
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Nomenclatura de hidrocarburos recomendaciones de la iupac 2004

Nomenclatura de hidrocarburos recomendaciones de la iupac 2004
Tabla Periodica, configuración electronica y electrones de valencia

Tabla Periodica, configuración electronica y electrones de valencia
Destacado (6)
Similar a Cómo obtener el nº de partículas subatómicas. ok
Similar a Cómo obtener el nº de partículas subatómicas. ok (18)
Atomoejerciciosresueltos3eso 150222103305-conversion-gate02

Atomoejerciciosresueltos3eso 150222103305-conversion-gate02
Atomoejerciciosresueltos3eso 150222103305-conversion-gate02

Atomoejerciciosresueltos3eso 150222103305-conversion-gate02
La estructura de la materia. Agrupaciones de átomos

La estructura de la materia. Agrupaciones de átomos
Más de Hogar
Más de Hogar (20)
Replicación del DNA. Guía basada en la metodología POGIL.pdf

Replicación del DNA. Guía basada en la metodología POGIL.pdf
Dogma central de la biología molecular. Guía basada en la metodología POGIL.pdf

Dogma central de la biología molecular. Guía basada en la metodología POGIL.pdf
¿cómo interactúan los seres vivos? Guía basada en la metodología POGIL..pdf

¿cómo interactúan los seres vivos? Guía basada en la metodología POGIL..pdf
Sistema circulatorio. Guía basada en la metodología POGIL.pdf

Sistema circulatorio. Guía basada en la metodología POGIL.pdf
Inmunidad en procariotas. Guía basada en la metodología POGIL.pdf

Inmunidad en procariotas. Guía basada en la metodología POGIL.pdf
Morfología cromosómica eucariota.Guía basada en la metodología POGIL.pdf

Morfología cromosómica eucariota.Guía basada en la metodología POGIL.pdf
Crispr cas9, edición del genoma. Guía basada en la metodología POGIL.pdf

Crispr cas9, edición del genoma. Guía basada en la metodología POGIL.pdf
Ciclo sars cov2-2021. Guía basada en la metodología POGIL.

Ciclo sars cov2-2021. Guía basada en la metodología POGIL.
Fotosíntesis, Guía basada en la metodología POGIL, para primeros medios

Fotosíntesis, Guía basada en la metodología POGIL, para primeros medios
Movimiento de los continentes, guía basada en la metodología POGIL.

Movimiento de los continentes, guía basada en la metodología POGIL.
Carrera armamentista entre los animales. Guía basada en la metodología POGIL

Carrera armamentista entre los animales. Guía basada en la metodología POGIL
Objetos de nuestro sistema solar. Guía basada en la metodología POGIL.

Objetos de nuestro sistema solar. Guía basada en la metodología POGIL.
¿Cómo funciona el Dna? Guía de biología octavo de enseñanza básica, 

¿Cómo funciona el Dna? Guía de biología octavo de enseñanza básica,
Chi-cuadrado, guía para biólogos, basada en la Metodología POGIL

Chi-cuadrado, guía para biólogos, basada en la Metodología POGIL
Ciclo de vida de las estrellas, guía basada en la metodología POGIL

Ciclo de vida de las estrellas, guía basada en la metodología POGIL
Análisis de secuencias de aminoácidos para determinar relaciones evolutivas

Análisis de secuencias de aminoácidos para determinar relaciones evolutivas
Último
Último (20)
Desarrollo y Aplicación de la Administración por Valores

Desarrollo y Aplicación de la Administración por Valores
RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION

RESOLUCIÓN VICEMINISTERIAL 00048 - 2024 EVALUACION
PP_Comunicacion en Salud: Objetivación de signos y síntomas

PP_Comunicacion en Salud: Objetivación de signos y síntomas
ACERTIJO LA RUTA DEL MARATÓN OLÍMPICO DEL NÚMERO PI EN PARÍS. Por JAVIER SOL...

ACERTIJO LA RUTA DEL MARATÓN OLÍMPICO DEL NÚMERO PI EN PARÍS. Por JAVIER SOL...
🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx

🦄💫4° SEM32 WORD PLANEACIÓN PROYECTOS DARUKEL 23-24.docx
Tema 10. Dinámica y funciones de la Atmosfera 2024

Tema 10. Dinámica y funciones de la Atmosfera 2024
Concepto y definición de tipos de Datos Abstractos en c++.pptx

Concepto y definición de tipos de Datos Abstractos en c++.pptx
La Sostenibilidad Corporativa. Administración Ambiental

La Sostenibilidad Corporativa. Administración Ambiental
Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO

Prueba de evaluación Geografía e Historia Comunidad de Madrid 4ºESO
Tema 19. Inmunología y el sistema inmunitario 2024

Tema 19. Inmunología y el sistema inmunitario 2024
Cómo obtener el nº de partículas subatómicas. ok
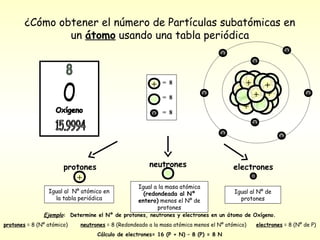
- 1. ¿Cómo obtener el número de Partículas subatómicas en un átomo usando una tabla periódica - - - + = 8 ++ + - + + + - = 8 + + - = 8 - - - protones neutrones electrones + - Igual a la masa atómica Igual al Nº atómico en (redondeada al Nº Igual al Nº de la tabla periódica entero) menos el Nº de protones protones Ejemplo: Determine el Nº de protones, neutrones y electrones en un átomo de Oxígeno. protones = 8 (Nº atómico) neutrones = 8 (Redondeado a la masa atómica menos el Nº atómico) electrones = 8 (Nº de P) Cálculo de electrones= 16 (P + N) – 8 (P) = 8 N
- 2. ¿Cómo obtener el número de Partículas subatómicas en un ión usando una tabla periódica - - - Note cómo dos 2- + = 8 - ++ + electrones + + + han sido = 8 - ganados por el = 10 8 + + - átomo, resultando - - así en un - ión protones neutrones electrones + - Igual al Nº de protones más el Nº de la Igual al número Igual a la masa atómica esquina superior derecha si es seguido atómico en la tabla (Redondeada al Nº entero) por a (-) O menos el Nº en la esquina periódica menos el Nº de protones superior derecha si es seguido por a (+) Ejemplo: Determine el Nº de protones, neutrones y electrones en el Ión Oxígeno O²¯. protones = 8 (Nº atómico) neutrones = 8 (masa atómica redondeada menos el Nº atómico) electrones = 10 Cálculo de Neutrones= 16 (P + N) – 8 (P) = 8 N Cálculo de electrones= 8 (e) + 2 (e) = 10
