Una explicación sencilla de la teoría de bandas en los sólidos
- 1. Una explicación sencilla de la teoría de bandas en los sólidos Por Francisco R. Villatoro, el 22 julio, 2015. Categoría(s): Ciencia • Física • Physics • Science ✎ 3 La teoría de bandas permite explicar la conducción de electricidad en los metales. En estos materiales las bandas de valencia (la última completamente ocupada por electrones a baja temperatura) y de conducción (la primera completamente vacía a baja temperatura) se cruzan, permitiendo que los electrones en estados de valencia se muevan como si fueran libres saltando a estados de conducción. Para explicar el por qué se requieren ciertos conocimientos de física cuántica. Los niveles energéticos de un electrón en un átomo se duplican en una molécula binaria, se triplican en una ternaria, y así sucesivamente se van multiplicando de forma sucesiva conforme se añaden átomos en un sólido. El resultado es que para trillones de átomos tenemos trillones de estados energéticos disponibles para los electrones. Me ha gustado cómo explica la teoría de bandas Chad Orzel, «Why Do Solids Have Energy Bands?,» Science, Forbes, 13 Jul 2015. Te recomiendo su lectura y te hago un resumen breve. Por cierto, te recomiendo también leer «Metals,» ChemPRIME, 13 Jan 2011.
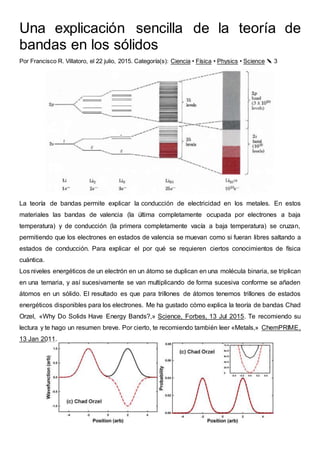
- 2. Para simplificar se supondrá un sistema en una sola dimesión. Imagina un electrón entre dos átomos cuyos centros se encuentran en las posiciones (arbitrarias) +2 y −2. Su función de onda cuántica puede ser de dos tipos: simétrica, estado bonding-bonding (figura izquierda, curva en negro), o antisimétrica, estado bonding-antibonding (figura izquierda, curva en rojo discontinua). La probabilidad de localizar el electrón es el cuadrado de su función de onda. Como muestra la figura de la derecha, en apariencia ambos estados tienen la misma distribución de probabilidad, con una región prohíbida en la parte central (en la que la probabilidad es muy pequeña). Ampliando la zona central se observa una pequeña diferencia entre ambos (ver inciso en la figura de la derecha comparando la curva negra y la roja discontinua). Esta pequeñísima diferencia impide que la energía de ambos estados sea degenerada, es decir, ambos estados deben tener una energía similar, pero diferente. De hecho, si hay dos electrones en lugar de uno, ocuparán estos dos estados diferentes sin problemas con el principio de exclusión de Pauli gracias a su diferencia de energía. En el caso de un electrón y tres átomos tenemos tres posibles estados no degenerados: bonding- bonding-bonding (curva en negro), bonding-antibonding-bonding (curva en verde) y bonding- bonding-antibonding (curva en rojo); otras combinaciones son degeneradas con respecto a éstas. Además, aparecen dos puntos (o zonas) prohíbidas entre ellos, en los que la probabilidad de localizar el electrón es muy pequeña. Las probabilidades de los tres estados posibles son parecidas, pero muestran pequeñas diferencias en los nodos (zonas prohibidas) entre los átomos. Conforme tenemos más átomos el número de posibles estados crece proporcionalmente al número de átomos y también crecen el número de puntos prohibidos. Como sus energías deben ser diferentes por el principio de exclusión de Pauli aparecerá una estructura de bandas casi continuas con regiones prohibidas entre ellas. Dentro de una banda las diferencias entre las distribuciones de probabilidad son muy pequeñas entre todos los estados posibles, luego las diferencias entre las energías de dichos estados son muy pequeñas. En la práctica las bandas son continuas. Lo más interesante es que aparecen bandas prohibidas
- 3. prohibidas que corresponden a las regiones donde la probabilidad de localizar a los electrones entre átomos es muy pequeña. Mi resumen del artículo de Orzel trata de reflejar su idea; si lees en inglés, te recomiendo leerle directamente. No te arrepentirás. Coda final. Esta entrada participa en la edición LXII del Carnaval de la Física cuyo blog anfitrión es La aventura de la ciencia.