Análisis Gravimétrico - Química
•
0 recomendaciones•21 vistas
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Más contenido relacionado
La actualidad más candente
La actualidad más candente (12)
7° práctica dirigida 4 to de secundaria (nomenclatura inorgánica_)

7° práctica dirigida 4 to de secundaria (nomenclatura inorgánica_)
Más de JoaquinMontoro
Más de JoaquinMontoro (20)
Uso del Cabello Humano Para Quitar el Petróleo del Mar - Química

Uso del Cabello Humano Para Quitar el Petróleo del Mar - Química
Último
Centros Multigrados Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...Katherine Concepcion Gonzalez
Último (20)
Concepto y definición de tipos de Datos Abstractos en c++.pptx

Concepto y definición de tipos de Datos Abstractos en c++.pptx
AFICHE EL MANIERISMO HISTORIA DE LA ARQUITECTURA II

AFICHE EL MANIERISMO HISTORIA DE LA ARQUITECTURA II
PIAR v 015. 2024 Plan Individual de ajustes razonables

PIAR v 015. 2024 Plan Individual de ajustes razonables
Tema 10. Dinámica y funciones de la Atmosfera 2024

Tema 10. Dinámica y funciones de la Atmosfera 2024
ACRÓNIMO DE PARÍS PARA SU OLIMPIADA 2024. Por JAVIER SOLIS NOYOLA

ACRÓNIMO DE PARÍS PARA SU OLIMPIADA 2024. Por JAVIER SOLIS NOYOLA
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
Procedimientos para la planificación en los Centros Educativos tipo V ( multi...

Procedimientos para la planificación en los Centros Educativos tipo V ( multi...
Análisis Gravimétrico - Química
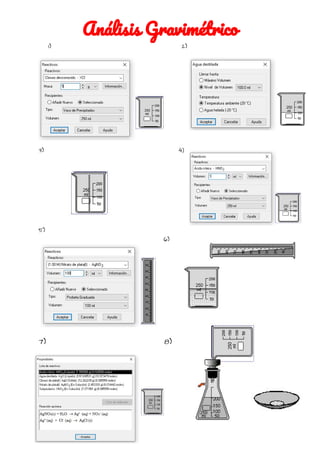
- 1. Análisis Gravimétrico 1) 2) 3) 4) 5) 6) 7)……………………………………...7) …………………………………………………8)
- 2. Análisis Gravimétrico Integrantes: -Joaquin Montoro -Andi Nuñez -Arellys Barba -Fabricio Castillo -Milka Ciurlizza -Jefferson Solorzano OBSERVACIONES: Masa de la muestra desconocida (g): 4g Masa del precipitado de AgCl: 9.8 g Volumen aproximado de disolución de AgNO3 añadido (mL): 100 ml 1. Moles de AgCl = (masa del precipitado de AgCl / 143,32): 9.8g /143,32= 0.0683 2. Masa de Cl- en la muestra de XCl = (moles de AgCl)x(masa atómica del Cl- = 35,4527): 0.0683 x 35.4527= 2.42. 3. % de Cl- en la muestra desconocida = (masa de Cl- en la muestra / masa de la muestra de XCl) x 100%: 2.42 / 4 = 60.5 % ¿Qué sucede con el exceso de AgNO3 añadido a la disolución? xcl + AgNO3 = Agcl + XNy areO3 M= 4 100 g 12.915 m=58.5 170 143.5 n=0.07 0.58 0.07 1:1 0.07 0.07 / 0.51 (exceso) (limitante)