Análisis Gravimétrico - Química
•
0 recomendaciones•82 vistas
Denunciar
Compartir
Denunciar
Compartir
Descargar para leer sin conexión
Recomendados
Recomendados
Reacciones de precipitación: Formación de precipitados y desplazamiento del e...

Reacciones de precipitación: Formación de precipitados y desplazamiento del e...Oswaldo Lescano Osorio
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
Determinación de cloruros por el método de volhard

Determinación de cloruros por el método de volhard
8° práctica dirigida 4 to de secundaria (unidades químicas de masa_)

8° práctica dirigida 4 to de secundaria (unidades químicas de masa_)
Volumetría por precipitación Equipo #6 Quimica Analitica 

Volumetría por precipitación Equipo #6 Quimica Analitica
Práctica. análisis cuantitativo de cationes. revisada 2

Práctica. análisis cuantitativo de cationes. revisada 2
PRACTICA # 7. DETERMINACIÓN DE CLORUROS MÉTODO DIRECTO

PRACTICA # 7. DETERMINACIÓN DE CLORUROS MÉTODO DIRECTO
Taller maestria contenidos 1 y 3-universidad nacional de colombia sede maniza...

Taller maestria contenidos 1 y 3-universidad nacional de colombia sede maniza...
Similar a Análisis Gravimétrico - Química
Reacciones de precipitación: Formación de precipitados y desplazamiento del e...

Reacciones de precipitación: Formación de precipitados y desplazamiento del e...Oswaldo Lescano Osorio
Similar a Análisis Gravimétrico - Química (20)
Guía de ejercicios - Análisis Químico - Unidad III 

Guía de ejercicios - Análisis Químico - Unidad III
Reacciones de precipitación: Formación de precipitados y desplazamiento del e...

Reacciones de precipitación: Formación de precipitados y desplazamiento del e...
Reacción química - 1.Unidades y estequiometría - Ejercicio 10 Cálculos de la ...

Reacción química - 1.Unidades y estequiometría - Ejercicio 10 Cálculos de la ...
Más de JoaquinMontoro
Más de JoaquinMontoro (20)
Uso del Cabello Humano Para Quitar el Petróleo del Mar - Química

Uso del Cabello Humano Para Quitar el Petróleo del Mar - Química
Último
Último (20)
Sesión de aprendizaje Planifica Textos argumentativo.docx

Sesión de aprendizaje Planifica Textos argumentativo.docx
ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA

ACERTIJO DE POSICIÓN DE CORREDORES EN LA OLIMPIADA. Por JAVIER SOLIS NOYOLA
ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx

ACUERDO MINISTERIAL 078-ORGANISMOS ESCOLARES..pptx
TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx

TIPOLOGÍA TEXTUAL- EXPOSICIÓN Y ARGUMENTACIÓN.pptx
Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 2do Grado Educacion Primaria 2024 Ccesa007.pdf
Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf

Planificacion Anual 4to Grado Educacion Primaria 2024 Ccesa007.pdf
ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...

ACERTIJO DE LA BANDERA OLÍMPICA CON ECUACIONES DE LA CIRCUNFERENCIA. Por JAVI...
Caja de herramientas de inteligencia artificial para la academia y la investi...

Caja de herramientas de inteligencia artificial para la academia y la investi...
proyecto de mayo inicial 5 añitos aprender es bueno para tu niño

proyecto de mayo inicial 5 añitos aprender es bueno para tu niño
MAYO 1 PROYECTO día de la madre el amor más grande

MAYO 1 PROYECTO día de la madre el amor más grande
Análisis Gravimétrico - Química
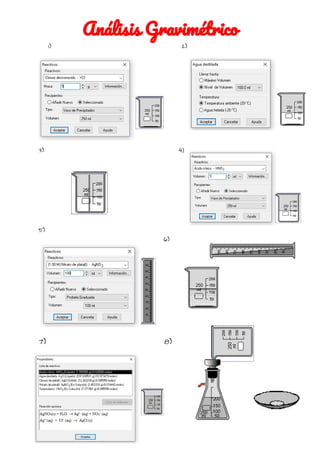
- 1. Análisis Gravimétrico 1) 2) 3) 4) 5) 6) 7)……………………………………...7) …………………………………………………8)
- 2. Análisis Gravimétrico Integrantes: -Joaquin Montoro -Andi Nuñez -Arellys Barba -Fabricio Castillo -Milka Ciurlizza -Jefferson Solorzano OBSERVACIONES: Masa de la muestra desconocida (g): 4g Masa del precipitado de AgCl: 9.8 g Volumen aproximado de disolución de AgNO3 añadido (mL): 100 ml 1. Moles de AgCl = (masa del precipitado de AgCl / 143,32): 9.8g /143,32= 0.0683 2. Masa de Cl- en la muestra de XCl = (moles de AgCl)x(masa atómica del Cl- = 35,4527): 0.0683 x 35.4527= 2.42. 3. % de Cl- en la muestra desconocida = (masa de Cl- en la muestra / masa de la muestra de XCl) x 100%: 2.42 / 4 = 60.5 % ¿Qué sucede con el exceso de AgNO3 añadido a la disolución? xcl + AgNO3 = Agcl + XNy areO3 m= 4 100 g 9.8 M=58.5 170 143.5 n=0.07 0.58 0.07 1:1 0.07 0.07 / 0.51 (exceso) (limitante)
- 3. Análisis Gravimétrico Rpta: El exceso del nitrato de plata va estar disuelto en agua, o sea en estado acuoso y por tal va ser filtrado dejando solo el componente sólido que queremos (precitado). 1. ¿De no disolverse previamente el cloruro del metal desconocido en agua podría llevarse a cabo el proceso de la determinación de cloruros? No, porque al no disolverse en agua no se podría precipitar ya que no pasaría de sólido a acuoso y por lo tanto no se podría llevar a cabo el proceso de determinación de cloruros. 2. Si pesaste 0.7527 g de cloruro de metal desconocido (XCl) al cual lo disuelves en agua y posteriormente lo tratas con una disolución de AgNO3. si al final del proceso pesaste 1.2354 g de precipitado.¿Calcula el rendimiento de la reacción y el porcentaje de la masa del Cl en el compuesto original? Masa de la muestra desconocida (g): 0.7527g Masa del precipitado de AgCl: 1.2354g Volumen aproximado de disolución de AgNO3 añadido (mL): 100 ml xCl + AgNO3 = AgCl + XNy areO3 m= 0.7527 100 g 1.2354 M= 87.52 170 143.5 n= 0.0086 0.58 0.0086 1:1 0.0086 0.0086 / 0.570.31 (exceso) (limitante)
- 4. Análisis Gravimétrico 0.0086 mol XCl = 0.0086 mol CL = m/M = 0.0086 = m/35.5 m CL-= 0.31 (g) m XCl= 0.7527 (g) = % Cl- = 0.31/0.7527 * 100% = 0.41%