Mapa
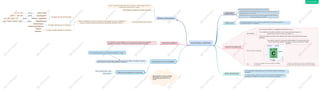
- 1. REACCIONES QUÍMICAS ¿QUÉ SON? MASA MOLECULAR BALANCEO DE ECUACIONES CONCEPTOS BÁSICOS ECUACIÓN QUÍMICA Procesos termodinámicos que transforman de la materia. Intervienen dos o más sustancias llamadas reactivos o reactantes, cambian significativamente en el proceso. Generalmente los cambios químicos producen sustancias nuevas, distintas de las que teníamos al principio. “La masa de los reactivos debe ser igual a la masa de los productos, esto implica que la cantidad y variedad de átomos presentes en los reactivos debe mantenerse en los productos. Peso atómico Masa atómica promedio Mol Es la masa de un átomo, en unidades de masa atómica (u.m.a). Una unidad de masa atómica se define como la masa exactamente igual a un doceavo de la masa de un átomo de carbono-12. Para medir la masa de un elemento se debe establecer la masa promedio de la mezcla natural de los isótopos, esta masa es la que se encuentra en la tabla periódica El mol es la unidad con que se mide la cantidad de sustancia Puede ser cualquiera de las siete magnitudes físicas fundamentales del Sistema Internacional de Unidades. Es la expresión en la que aparecen como sumando las fórmulas de los reactantes, seguidos de una flecha, y las fórmulas de los productos también sumándose. CLASIFICACIÓN DE REACCIONES Dada la variedad de reacciones químicas hay bastantes formas de clasificarlas. Vamos a estudiar diversas clasificaciones atendiendo diferentes criterios. ¿Sabías qué? REACCIÓN QUÍMICA Ocurre cuando las moléculas de los reactivos rompen algunos de sus enlaces para formar otros nuevos. Esto conlleva a la aparición de nuevas sustancias. El átomo de carbono se utiliza como referencia para medir la masa atómica de los demás elementos Es la suma de las masas atómicas en una molécula, también llamado peso molecular. Su valor numérico coincide con el de la masa molar, pero habitualmente expresado en unidades de masa atómica, en lugar de gramos/mol. Las reacciones químicas son muy comunes y pueden darse de manera espontánea, en condiciones diversas en la naturaleza A) Según tipo de transformación B) Según partículas que se transfieren C) Según energía implicada en el proceso Es una consecuencia de la ley de la conservación de la masa de A. Lavoisier: Métodos para balancear ecuaciones Balancear significa encontrar los coeficientes estequiométricos en una reacciónencontrar los coeficientes estequiométricos en una reacción Método Inspección simple o Tanteo Método Algebraico Síntesis ,o, adición Descomposición Sustitución, o , desplazamiento Desplazamiento doble Acido-base Protones Oxidación-reducción Electrones Exotérmica Endotérmica EjemploFe + S = Fes EjemploCaCO3 ------- CaO + CO2 Ejemplo Ejemplo Na + H20 = NaOH + H2 NaCl + CaNO3 = NaNO3 + CaCl2