Enlaces quimicos
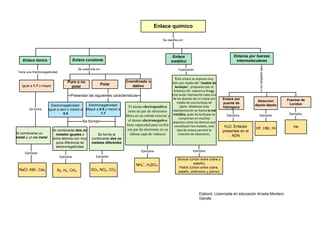
- 1. Enlace químico Se clasifica en: Enlace Enlaces por fuerzas Enlace iónico Enlace covalente metálico intermoleculares Se clasifican en: Se subdivide en: Explicación Tiene una Electronegatividad Este enlace se expresa muy Puro o no Coordinado o bien por medio del “modelo de Igual a 1.7 o mayor Polar dativo polar burbujas”, propuesto por el británico Sir. Lawrence Rragg. Presentan las siguientes características Este autor representó cada uno de los átomos de un metal por Enlace por Fuerzas de medio de una burbuja de Atracción puente de London Electronegatividad: Electronegatividad: El átomo electropositivo jabón. Mediante esta dipolo-dipolo hidrógeno Se forma igual a cero o menor a Mayor a 0.5 y menor a representación se ilustra la red tiene un par de electrones 0.5 1.7 Ejemplos libres en un orbital exterior y metálica, pues las burbujas se Ejemplos Ejemplos comportan en muchos Se forman el átomo electronegativo aspectos como los átomos que tiene capacidad para recibir constituyen los metales, este H2O, Enlaces He ese par de electrones en su tipo de enlace permite la HF, HBr, HI Al combinarse dos no presentes en el Al combinarse un metales iguales o Se forma al última capa de valencia creación de aleaciones. metal y un no metal ADN entre átomos con muy combinarse dos no poca diferencia de metales diferentes electronegatividad Ejemplos Ejemplos Ejemplos Ejemplos Ejemplos Bronce (Unión entre cobre y NH4+, H2SO4 estaño) Peltre (Unión entre cobre, NaCl, KBr, CaI2 N2, H2, CH4 SO3, NO2, CO2 estaño, antimonio y plomo) Elaboró: Licenciada en educación Arcelia Montero Garcés
