Formulario de Química
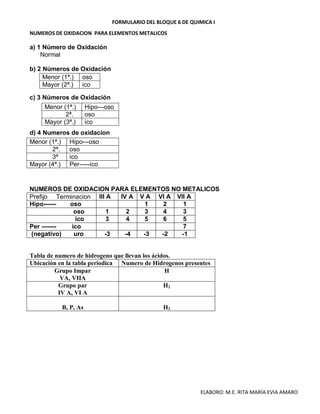
- 1. FORMULARIO DEL BLOQUE 6 DE QUIMICA I ELABORO: M.E. RITA MARÍA EVIA AMARO NUMEROS DE OXIDACION PARA ELEMENTOS METALICOS a) 1 Número de Oxidación Normal b) 2 Números de Oxidación c) 3 Números de Oxidación d) 4 Numeros de oxidacion NUMEROS DE OXIDACION PARA ELEMENTOS NO METALICOS Prefijo Terminacion III A IV A V A VI A VII A Hipo------ oso 1 2 1 oso 1 2 3 4 3 ico 3 4 5 6 5 Per ------- ico 7 (negativo) uro -3 -4 -3 -2 -1 Tabla de numero de hidrogeno que llevan los ácidos. Ubicación en la tabla periodica Numero de Hidrogenos presentes Grupo Impar VA, VIIA H Grupo par IV A, VI A H2 B, P, As H3 Menor (1ª.) oso Mayor (2ª.) ico Menor (1ª.) Hipo---oso 2ª. oso Mayor (3ª.) ico Menor (1ª.) Hipo---oso 2ª. oso 3ª ico Mayor (4ª.) Per-----ico
- 2. FORMULARIO DEL BLOQUE 6 DE QUIMICA I ELABORO: M.E. RITA MARÍA EVIA AMARO TABLA II: FORMULAS Y NOMENCLATURAS DE LAS DIVERSAS FUNCIONES Función Quimica Formula Nomenclatura Ginebra Nomenclatura IUPAC 1. Oxido Basico + -2 M O oso Oxido metal ico Oxido de metal (NR) 2. Anhidridos + -2 NmO hipo oso Anhídrido Nm per ico Anhidrido de Nm (NR) 3. Hidroxido + -1 M (OH) oso Hidróxido metal ico Hidroxido de Metal (NR) 4. Hidruro Metalico + -1 M H oso Hidruro metal ico Hidruro de Metal (NR) 5. Hidruro no Metalico - + NmH Hidruro de no metal 6. Acido Hidracido + - HNm Acido Nm hídrico Nmuro de hidrogeno 7. Oxiacido + - -2 HNmO hipo oso Acido Nm per ico ito Nm de Hidrogeno ato 8. Sal binaria + - MNm oso Nmuro de metal ico Nmuro de metal (NR) 9. Oxisal + - -2 MNmO ito oso Nm de Metal Ato ico ito Nm de Metal (NR) ato 10. Sal binaria Acida + + - MHNm oso Nmuro acido de metal ico Nmuro acido de metal (NR) 11. Oxisal Acida + + - -2 MHNmO ito oso Nm acido de Metal ato ico ito Nm acido de Metal (NR) ato M = Metal NR = números romanos Nm = No metal H = hidrogeno O = oxigeno
- 3. FORMULARIO DEL BLOQUE 6 DE QUIMICA I ELABORO: M.E. RITA MARÍA EVIA AMARO TABLA DE RADICALES COMUNES E IMPORTANTES Grupo VIIA F, Cl, Br, I El fluor (f), el bromo (Br), y el yodo (I), dan radicales similares al cloro (Cl) F-1 Cl -1 Br -1 I -1 ClO -1 ClO2 -1 ClO3 -1 ClO4 -1 Fluoruro Cloruro Bromuro Yoduro Hipoclorito Clorito Clorato Perclorato Con Metales de transicion CrO4 -2 Cr2O7 -2 MnO4 -2 MnO4 -1 Fe( CN)6 -3 Fe( CN)6 -4 ZnO2 -2 MoO4 -2 TiO4 -4 Cromato Dicromato Manganato Permanganato Ferricianuro Ferrocianuro Zincato Molibdato Titanato Radicales positivos H3O+1, H+1 NH4 + PH4 + AsH4 Hidronio Amonio Fosfonio Arsonio Grupo IIIA BO3 -3 BO2 -3 HBO3 -2 H2BO3 -1 HBO2 -2 H2BO2 -1 Borato Borito Borato acido Borato diacido Borito acido Borito diacido Grupo IV A C, Si CO3 -2 CO2 -2 HCO3 - HCO2 - SIO3 -2 CN- CNO- Carbonato Carbonito Carbonato ácido o bicarbonato Carbonito ácido Silicato Cianuro Cianato Grupo V A N, P, As El Arsénico (As), da radicales similares al Fósforo (P) N-3 P-3 As-3 NO2 -1 NO3 -1 PO2 -3 PO3 -3 PO4 -3 HPO2 -2 HPO3 -2 HPO4 -2 H2PO2 -1 H2PO3 -1 H2PO4 -1 Nitruro Fosfuro Arsenuro Nitrito Nitrato Hipofosfito Fosfito Fosfato Hipofosfito ácido Fosfito ácido Fosfato ácido Hipofosfito diácido Fosfito diácido Fosfato diácido Grupo VI A S, Se, Te El selenio (Se), y el telurio (Te), dan radicales similares al Azufre(S) O-2 OH-1 S-2 Se-2 Te-2 HS-1 SO2 -2 SO3 -2 SO4 -2 HSO2 -1 HSO3 -1 HSO4 -1 S2O3 -2 SCN-1 Oxido Hidróxido Sulfuro Selenuro Telururo Sulfuro ácido Hiposulfito Sulfito Sulfato Hiposulfito ácido Sulfito ácido o Bisulfito Sulfato ácido o bisulfato Tiosulfato Sulfocianuro o tiacanato
