Este documento describe diferentes tipos de compuestos binarios de oxígeno, incluyendo óxidos metálicos, óxidos no metálicos, óxidos neutros, peróxidos e hidruros metálicos y no metálicos. Explica las fórmulas, nomenclaturas y ejemplos de cada tipo de compuesto. También incluye ejercicios para practicar la escritura de fórmulas y nombres de compuestos.

![ÓXIDOS METÁLICOS - ÓXIDOS BÁSICOS
Compuestos binarios formados por: Oxígeno
(-2)+ Metal.
Fórmula: M+
+ O-2
(Siendo M: metal; O: oxígeno).
Para escribir la fórmula se escribe el M seguido del O y
se intercambian los números de oxidación. Se
simplifican los subíndices en el caso necesario.
-Nomenclatura:
Tradicional: Óxido + [metal]
Stock: Óxido de [metal] (valencia en nº romanos).
Sistemática: + óxido de + [metal]
oso – menor valencia
ico – mayor valencia
Mono-
Di-
Tri-
Tetra-
Mono -
Di -](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-2-320.jpg)




![-Nomenclatura:
Tradicional: Óxido + + [no metal] +
Stock: Óxido de [ no metal] (valencia en nº
romanos).
Sistemática: + óxido de + [no metal]
* Para más facilidad leer la fórmula al revés.
-oso
-oso
-ico
-ico
Hipo-
Per-
Mono-
Di-
Mono-
Di-
Tri-
Tetra-](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-7-320.jpg)




![PERÓXIDOS
• Compuestos binarios formados por: Oxígeno (-1)+
Metal
• Fórmula: M+
+ O-1
(Siendo O: oxígeno; M: metal)
• Se forman especialmente con los metales de valencia
+1 y +2
• En el caso de que la valencia del metal sea igual a 1,
se pone subíndice 2 tanto al metal como al oxígeno y
no se simplifica.
Nomenclatura:
• Tradicional: Peróxido + metal (valencia variable oso –
ico)
• Stock: Peróxido de [metal] (valencia del metal con no
romanos)
• Sistemática: utilización de prefijos (mono, di, tri, etc.)](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-12-320.jpg)


![HIDRUROS METÁLICOS
Compuestos binarios formados por: Hidrógeno(-1)+
Metal.
Fórmula: M+
+ H-1
(Siendo M: metal; H: hidrógeno).
Para escribir la fórmula se escribe el M seguido del H y se
intercambian los números de oxidación.
-Nomenclatura:
Tradicional: Hidruro + [metal] +
Stock: Hidruro de [metal] (valencia en nº romanos).
Sistemática: + hidruro de [metal]
Mono-
Di-
Tri-
Tetra-
-oso
-ico](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-15-320.jpg)
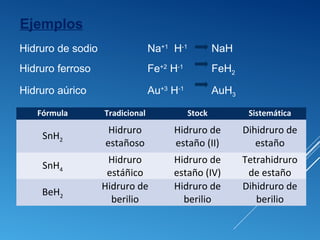


![Compuestos binarios formados por: Hidrógeno(+1)+ No
Metal (-)
Fórmula: H+1
NM-
(Siendo H: hidrógeno y NM: no metal).
Nomenclatura:
Tradicional: Ácido + [no metal] - hídrico
Stock: [no metal] – uro de hidrógeno.
Sistemática: (mono) + [no metal] – uro de (mono – di
) hidrógeno
HIDRUROS NO METÁLICOS – ÁCIDOS
HIDRÁCIDOS](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-19-320.jpg)


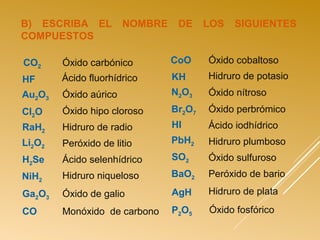
![COMPUESTOS ESPECIALES
Compuestos binarios formados por: Hidrógeno(-1)+ No
Metal
Fórmula: NM+
+ H-1
(Siendo NM: no metal; H: hidrógeno).
Nomenclatura:
• Tradicional: nombre especial
• Stock: Hidruro de [no metal] (valencia en nº
romanos).
• Sistemática: + hidruro de [no metal]
-Grupos 13 y 15, valencia 3
-Grupo 14, valencia 4
-Tri
-Tetra](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-24-320.jpg)
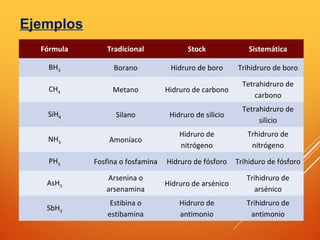
![HIDRÓXIDOS O BASES
Compuestos ternarios formados por: Metal + grupo
(OH) (-1)
Fórmula: M+
(OH)-1
(Siendo M: metal y OH: grupo
hidróxido;).
- Nomenclatura:
Tradicional: HIdróxido + [metal]
Stock: Hidróxido de [metal] (valencia del metal)
Sistemática: + hidróxido de [metal]
Mono-
Di-
Tri-
Tetra-
-oso
-ico](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-26-320.jpg)
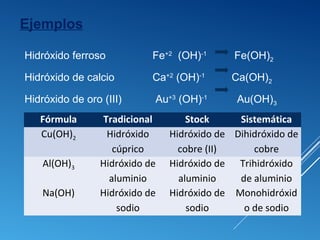


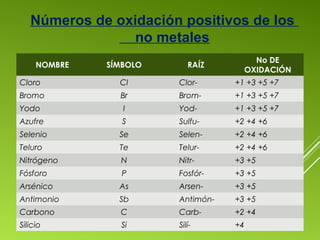
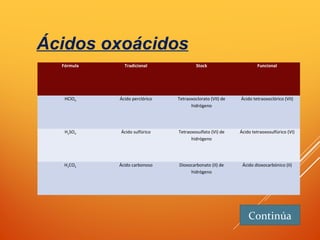
![ÁCIDOS OXÁCIDOS
Compuestos ternarios formados por: Hidrógeno , No
Metal y Oxígeno
Fórmula General: H+1
a NM+
bO-2
c
Resultan de la combinación de una molécula de
óxidos no metálicos o anhídridos con una molécula de
agua.
Óxido hipocloroso: Cl2O + H2O = HClO
- Nomenclatura:
Tradicional: Ácido + [no metal]
Hipo-
Per-
-oso
-oso
-ico
-ico](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-30-320.jpg)



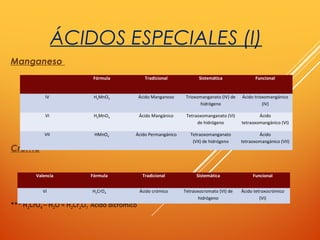

![SALES BINARIAS (SALES
NEUTRAS)
- Compuestos binarios formados por: Metal+ No Metal
- Fórmula: M val X Xval M (Siendo X: no metal; M: metal).
-Si se pueden simplificar los subíndices, se simplifican. Los subíndices siempre son
números naturales (jamás un número fraccionario o decimal como subíndice).
- Nomenclatura:
Tradicional: [no metal] – uro de [metal]
Stock: [no metal] – uro de[metal] (valencia del metal)
Sistemática: + [no metal] – uro de + [metal]
* Para más facilidad leer la fórmula al revés.
Grupo 17 (F, Cl, Br, I), valencia 1
Grupo 16 (S, Se, Te), valencia 2
Mono-
Di-
Tri-
Tetra-
Mono-
Di-
-oso
-ico
Ejemplos](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-38-320.jpg)
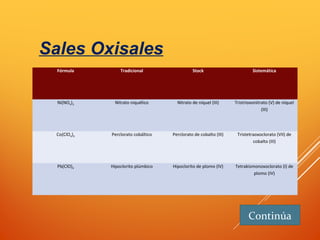
![SALES OXISALES
- Compuestos ternarios formados por: Metal + No Metal + Oxígeno
- Fórmula: M a (XbOc )val M
Cambiamos el oxígeno por un metal y ponemos su valencia fuera del paréntesis. El subíndice que
tiene el hidrógeno se deja.
Nomenclatura:
Tradicional: [no metal] [ metal]
Stock: [no metal] de [ metal]
Sistemática: + oxo [no metal] - ato (val X) de [metal] (val M)
* Para más facilidad leer la fórmula al revés.
Hipo-
Per-
-ito
-ito
-ato
-ato
-oso
-ico
Hipo-
Per-
-ito
-ito
-ato
-ato
Bis-
Tris-
Tetrakis-
Mono-
Di-
Tri-
Tetra-
Ejemplos](https://image.slidesharecdn.com/nomenclaturaquimica-160902173647/85/Nomenclatura-quimica-40-320.jpg)